Вычисление - летучесть
Cтраница 2
Стандартным состоянием при вычислении летучести всегда является состояние идеализированного газа при давлении в одну атмосферу. Но в ряде случаев этот выбор стандартного состояния невозможен или нецелесообразен. Однако при любом другом выборе стандартного состояния, от которого отсчитывают значения химического потенциала, получают уже не летучесть, а другую величину - активность. [16]
Рассмотрим наиболее применяемые способы вычисления летучести. [17]
Существует ряд простых способов вычисления летучестей и коэффициентов летучестей реальных газов ( и компонента в смеси реальных газов) по опытным данным зависимости объема газа от давления и температуры. [18]
На основе измерений и вычислений летучести реальных газов были определены по формуле (10.12) и сопоставлены с эффектами Джоуля - Том-сона энтальпии Я молекулярного взаимодействия в газах. [20]
Не останавливаясь на различных способах вычисления летучести чистых газов по данным о сжимаемости газов, отметим, что применение принципа соответственных состояний дает возможность приближенного нахождения значений коэффициента летучести в довольно значительном интервале приведенных температур и давлений. [21]
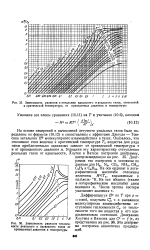
Уравнение ( 30) позволяет производить вычисление летучестей с достаточной для практических целей точностью только в случае не очень высоких давлений. Однако при давлениях порядка сотен атмосфер, даже для газов, находящихся при высоких по сравнению с критической температурах, применение указанного уравнения приводит, как это следует из данных табл. 1, к значительным неточностям. [22]
Расчет парожидкостного равновесия по уравнению состояния сводится к вычислению летучести ( или коэффициента летучести), а также коэффициентов активности компонентов газовой и жидкой фаз. Точность расчета коэффициентов распределения определяется точностью используемого уравнения состояния. [23]
Как для отыскания свойств реальных газов следует обратиться к вычислению летучести, так в случае растворов центр тяжести переносится на вычисление активности. Нахождение связи между активностью, с одной стороны, и температурой, давлением и концентрацией, с другой, делает возможным применение термодинамических закономерностей к реальным растворам. [24]
Поправочный множитель z, называемый коэффициентом сжимаемости, играет важную роль не только при расчете свойств системы, но и при вычислении летучести. Как вытекает из определяющего уравнения, коэффициент сжимаемости - безразмерная величина и, как показывает опыт, зависит от давления, температуры и природы вещества. [25]
Таким образом, замена р на f - формальный метод, где все трудности, связанные с отклонением газов от состояния идеального газа, переносятся на вычисление летучести. [26]
Константа равновесия реакции К по величине очень близка Kf при давлении 1 ат и ниже, а в некоторых случаях при давлении нескольких десятков атмосфер. Вычисление летучести чистых газов, как будет показано далее, не очень сложно. Определение же парциальной летучести газов в смеси представляет собой сложную и пока нерешенную задачу. [27]
При вычислении летучести стандартным состоянием всегда является состояние идеализированного газа при давлении в одну атмосферу. Из-за различия в стандартных состояниях летучесть чистого вещества в состоянии насыщенного пара не равна активности этого вещества в жидкой фазе, равновесно сосуществующей с газовой фазой. [28]
При вычислении летучести стандартным состоянием всегда является состояние идеализированного газа при давлении в одну атмосферу. [29]
Здесь не место обсуждать случаи, когда в опубликованных расчетах напрасно была отброшена величина Ap f или она была определена чрезмерно упрощенно, посредством столь грубых приемов, которые дают в сущности превратное представление об этой величине. Некоторые замечания по этому вопросу будут сделаны в разделе о вычислении летучести. [30]
Страницы: 1 2 3