Гибель - атом
Cтраница 3
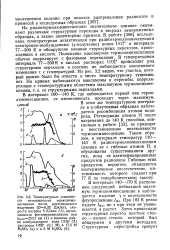
Таким образом, система С12 О2 обратима при облучении светом, и только при помощи метода импульсного фотолиза можно непосредственно наблюдать образование короткоживущих радикалов и исследовать их превращения. Другим примером наблюдения простых свободных радикалов могут служить образование и гибель атомов йода при облучении молекулярного йода. [31]
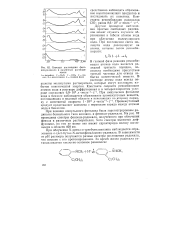 |
Спектры поглощения фенокси-радикала в различных растворителях. [32] |
Константа рекомбинации радикалов СЮ - равна 8 6 - 107 л-моль - - с-1. Другим примером наблюдения простых свободных радикалов может служить изучение образования и гибели атомов иода при облучении молекулярного иода. [33]
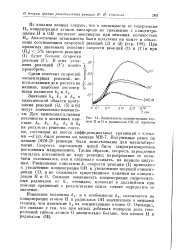 |
Зависимость концентрации атомов Н и О и радикалов ОН от времени. [34] |
Изменение величины А4, и в особенности Ае, сказывается на концентрации атомов Н и радикалов ОН значительно в меньшей степени, чем изменение А 5 на концентрацию атомов О. Очевидно, это связано с тем, что при малых добавках водорода роль гетерогенной гибели атомов О значительно больше, чем атомов Н и радикалов ОН. [35]
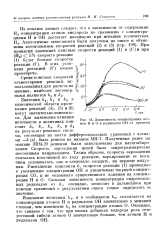 |
Зависимость концентрации атомов Н и О и радикалов ОН от времени. [36] |
Изменение величины А4, и в особенности А6, сказывается на концентрации атомов Н и радикалов ОН значительно в меньшей степени, чем изменение А5 на концентрацию атомов О. Очевидно, это связано с тем, что при малых добавках водорода роль гетерогенной гибели атомов О значительно больше, чем атомов Н и радикалов ОН. [37]
Отсюда видно, что при давлениях порядка 10 мм рт. ст. и ниже первое слагаемое в знаменателе формулы ( VI II. При давлениях порядка атмосферного и выше соотношение между этими слагаемыми изменяется на обратное, и гибель атомов Н на стенке происходит в диффузионной области. [38]
Описан масс-спектрометр, в котором ионизационная камера может охлаждаться до низкой температуры циркулирующим жидким азотом. Газы, диффундирующие из малого отверстия в стегано реактора, попадают прямо в ионизационную камеру, расположенную на расстоянии 8 мм от реактора. Масс-спектрометр был применен для изучения путей гибели атомов и свободных радикалов при столкновениях с металлическими стенками, находящимися при низкой контролируемой температуре. [39]
На рисунке показаны значения так называемого коэффициента рекомбинации атомов - у в изученном интервале температур. Видно, что этот коэффициент не является, в сущности, константой, а зависит к иже 200 К от давления. Тем более не является константой коэффициент гибели атомов на стенке, который часто рассматривается в кинетических схемах цепных реакций. [40]
На положение предела менее сильно влияют добавки углеводородов. Ингибирующее действие малых добавок примесей хорошо объясняется объемной гибелью атомов Н в реакции с примесями. [41]
Тормозящее действие примесей ( ингибиторов) на цепные реакции в большом числе случаев сводится к обрыву депей, обусловленному гибелью активных центров, в результате чего длина цепи может уменьшиться настолько, что реакция потеряет цепной характер. При изучении действия азота и кислорода на скорость образования НС1 Маркевич [233] показал, что в отличие от азота примесь кислорода сильно уменьшает скорость реакции, что объясняется обрывом цепей в результате реакции атомов хлора с молекулами кислорода. По-видимому, таков же ( возможно, связанный также с гибелью атомов водорода) механизм действия на эту реакцию треххлористого азота NC13, являющегося одним из наиболее активных ингибиторов реакции хлора с водородом. [42]
Это различие в зависимости скорости реакции и Y от / я может служить одним из первых и существенных указаний на характер развивающейся фотохимической реакции. Именно, если скорость реакции пропорциональна или общий квантовый выход обратно пропорционален квадратному корню из скорости по: глощения света, то важную роль в механизме играет рекомбинационный процесс второго порядка в отношении соответствующих атомов или радикалов. Можно даже утверждать, что в этом случае главнейшим, почти единственным, процессом гибели атомов или радикалов является рекомбинация в объеме. [43]
Это различие в зависимости скорости реакции и f от 1а может служить одним из прямых и существенных указаний на характер развивающейся фотохимической реакции. Именно, если скорость реакции пропорциональна или общий квантовый выход обратно пропорционален квадратному корню из скорости поглощения света, то важную роль в механизме играет рекомбинационный процесс второго порядка в отношении соответствующих атомов или радикалов. Можно даже утверждать, что в этом случае главнейшим, почти единственным, процессом гибели атомов или радикалов является рекомбинация в объеме. [44]
Страницы: 1 2 3 4