Гидрат
Cтраница 4
Гидрат СаС12 6Н2О при 293 К имеет давление пара воды 333 Па. При той же температуре давление пара воды над насыщенным раствором составляет 1000 Па. При каких условиях соль начинает расплываться. [46]
Гидраты относятся к неустойчивым молекулярным соединениям, сравнительно быстро разлагающимся на свои составные части - углеводород и воду. По внешнему виду они похожи на белую снегообразную кристаллическую массу; при уплотнении напоминают лед. [47]
 |
Прибор для возгонки трехокиси. [48] |
Гидрат можно легко получить или путем растворения металлической сурьмы в азотной кислоте с последующим выпариванием кислоты, или гидролизом пентахлорида сурьмы. Выше этой температуры происходит постепенное отщепление кислорода и продукт загрязняется четырехокисью сурьмы. При прокаливании ниже 270 процесс дегидратации может не дойти до конца. [49]
Гидраты образуются с выделением, а разлагаются с поглощением тепла. Теплота гидратообразования углеводородов составляет около 400 кДж / кг. [50]
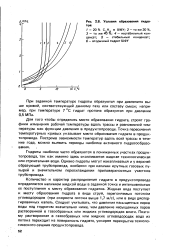 |
Условия образования гидратов. [51] |
Гидраты наиболее часто образуются в пониженных участках продук-топровода, так как именно здесь скапливается жидкая технологическая или строительная вода. Однако гидраты могут накапливаться и у верхней образующей трубопровода, особенно при наличии крупных газовых пузырей и значительном переохлаждении приповерхностных участков трубопровода. [52]
Гидрат этого окисла образуется в виде темно-коричневого осадка при действии щелочей на растворы солей трехвалентного титана. Он начинает осаждаться из кислых растворов при рН4, имеет только основные свойства и в избытке щелочи не растворяется. Однако производящиеся от HTiOa титаниты некоторых металлов ( Li, Na, Mg, Mn) были получены сухим путем. Известна также сине-черная титановая бронза ( ср. [53]
Гидраты способны образовывать связь газ-вода с большинством молекул, которые из газа могут перейти в раствор, образуемый за счет наличия конденсата воды в газе. Поэтому H2S и С02 ускоряют образование гидратов, особенно при повышенных температурах, так как они лучше растворимы в воде, чем углеводороды. [54]
Гидраты окислов и их систематика, основанная на проявлении в них химического сродства. [55]
Гидраты окислов называются гид роке идами. [56]
Гидраты этих окислов Со ( ОН) 2 и Со ( ОН) 3 нерастворимы в воде и обладают основными свойствами. При действии кислот на Со ( ОН) а получаются соли двухвалентного кобальта. [57]
Страницы: 1 2 3 4