Фенильное кольцо
Cтраница 2
Заместители в пара-положении фенильных колец вызывают небольшое изменение распределения спиновой плотности в радикале. [16]
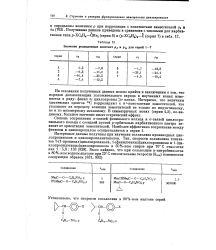 |
Значение реакционных констант pj и рд для серий 1 - 7. [17] |
Степень сопряжения я-связей фенильного кольца и сг-связей циклопро-пильного кольца с соседней пустой / ьорбиталью карбкатионного центра зависит от ориентации заместителей. [18]
Если в яара-положение фенильного кольца в 4-фенилазулене ( XLIII) или 4, 8-дифенилазулене ( XLIV) ввести сильную элек-тронно-донориую группу типа диметиламиногруппы ( с образованием соединений XLVI или XLVII), то на основании изложенных в разделе IV - А - 1 ( 3) соображений следует ожидать дополнительного гипсохромного сдвига. [19]
Введение в орто-положение фенильного кольца ациламиногруппы не только увеличивает интенсивность люминесценции, но и смещает максимум излучения в длинноволновую область более чем на 100 нм. В той же работе отмечается, что соединения этого ряда, содержащие амидную группу CONH, обладают двумя максимумами люминесценции в синей и желтой областях спектра. [20]
Разрыв связи между фенильным кольцом и индольным ядром, отвечающий образованию иона ( М - 77), будучи совершенно не характерным для фенилиндолов, в случае З - метил-2 - фенил - и 2-ме-тил - 3-фенилиндола реализуется в значительной степени. [21]
Влияние заместителя в фенильном кольце олово - и свинецорганических соединений в общем соответствует их влиянию в ароматическом электрсфильном замещении, однако при детальном рассмотрении обнаруживаются определенные отклонения. Так, влияние как активирующих, так и пассивирующих групп оказалось значительно меньшим не только по сравнению с электрофильным замещением в обычных ароматических соединениях, но и сравнительно с протоли-зом кремний - и германийорганических соединений. В отдельных группах заместителей также наблюдаются отличия. [22]
Значения PQ в фенильных кольцах рассчитывали по уравнению Мак-Коинела с Q - 27 э; Рст найдено из условия нормировки. [23]
Все заместители в фенильном кольце ( кроме трет, бутила) увеличивают его способность к присоединению фенильного радикала. Исследовано анти-радное действие ( 3-нафтиламина, фенил - 3-нафтиламина, дифениламина и трифениламина. [24]
Непосредственное введение заместителей в фенильное кольцо у атома олова обычно осуществить не удается. [25]
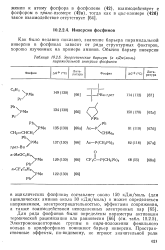 |
Энергетические барьеры ( в кДж / моль пирамидальной инверсии фосфинов. [26] |
Электроноакцепторные группы в пара-положении фенильного кольца в арилфосфинах понижают барьер инверсии. [27]
При этом у каждого фенильного кольца по крайней мере один из алкильных радикалов должен быть трет-бутильным, например 3 3 5 5 -тетра-грег - бутил-1 1 -диоксидифенил и 3 3 -диметил - 5 5 -ди-грег - бутил-1 1 -диоксидифенил. [28]
Константы СТВ с протонами фенильных колец в ДФМ и орто-замещенных ДФМ отличаются мало. [29]
Учет изменения углов поворота фенильных колец значительно улучшает согласие результатов расчета с опытом. [30]
Страницы: 1 2 3 4