Четырехкоординационный комплекс
Cтраница 1
Четырехкоординационные комплексы МА2В2 могут иметь квадратное или тетраэдрическое строение. Для квадратных комплексов возможны два геометрических изомера, тогда как для тетраэдриче-ского строения существование геометрических изомеров невозможно. Таким образом, изомеры соединений с координационным числом комплексообразователя 4 могут иметь только квадратное строение. Выводы Вернера впоследствии были подтверждены экспериментально и теоретически на основе квантовомеханических представлении. [1]
Четырехкоординационные комплексы МА2В2 могут иметь квадратное или тетраэдрическое строение. Для квадратных комплексов возможны два геометрических изомера, тогда как для тетраэдриче-ского строения существование геометрических изомеров невозможно. Таким образом, изомеры соединений с координационным числом комплексообразователя 4 могут иметь только квадратное строение. Выводы Вернера впоследствии были подтверждены экспериментально и теоретически на основе квантовомеханических представлений. [2]
Четырехкоординационные комплексы МА2В2 могут иметь плоское квадратное или тетраэдрическое строение. Для квадратных комплексов возможны два геометрических изомера, тогда как для тетраэдри-ческого строения существование геометрических изомеров невозможно. Таким образом, изомеры соединений с координационным числом комплексообразователя 4 могут иметь только квадратное строение. [3]
 |
Период полуобмена воды для гидратированных ионов металлов. [ По данным статьи М. Е i g е п, Pure Appl. [4] |
Четырехкоординационные комплексы ( как тетраэдриче-ские, так и плоские квадратные) реагируют в основном быстрее, чем аналогичные шестикоординационные системы. [5]
Четырехкоординационные комплексы МАгВг могут иметь квадратное или тетраэдрическое строение. Для квадратных комплексов возможны два геометрических изомера, тогда как для тетраэдрического строения существование геометрических изомеров невозможно. Таким образом, изомеры соединений с координационным числом комплексообразователя 4 могут иметь только квадратное строение. Выводы Вернера впоследствии были подтверждены эксперт ментально и теоретически на основе квантово-механических представлений. [6]
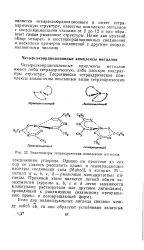 |
Энантиомеры тетраэдрических комплексов металлов. [7] |
Четырехкоординационные комплексы металлов имеют либо тетраэдрическую, либо плоскую квадратную структуру. [8]
Четырехкоординационные комплексы палладия ( II) с основаниями Шиффа способны дополнительно комплексоваться с двумя молекулами 1 3 5-тринитробензола. При этом не происходит, как можно было ожидать, изменения координационного числа палладия. [9]
Для четырехкоординационных комплексов по сравнению с шестью координированными обмен осуществляется быстрее. Здесь особую роль играет образование ионных связей центральный ион - лиганд в отличие от октаэдрических комплексов, где на энергию активации в большей степени оказывает влияние разрыв этой связи. Кинетическое поведение для этих двух групп комплексов в связи с этим заметно различается. [10]
Для многих четырехкоординационных комплексов переходных металлов наблюдаются быстрые [309] перегруппировки координационных полиэдров, хотя четырехкоординационные стереохими-чески лабильные гидриды не известны. [11]
 |
Схема структуры тримера ацетилацетоната никеля. [12] |
Мономер-полимерные равновесия, Четырехкоординационные комплексы могут ассоциировать или полимеризоваться с образованием пяти - и шестикоординационных соединений. В некоторых случаях ассоциация протекает столь сильно, что мономеры с координационным числом 4 наблюдаются лишь при высоких температурах. В других случаях положение равновесия таково, что при температурах вблизи комнатной в растворах могут сосуществовать красные диамагнитные мономеры и зеленые или синие полимеры, соотношение которых зависит от температуры и концентрации. В результате того, что некоторые из атомов кислорода в этом соединении выступают как мостиковые, каждый из атомов никеля приобретает октаэдрическую координацию. Этот три-мер очень устойчив, и заметные количества мономера в некоординирующемся растворителе обнаруживаются лишь при температурах около 200 С. Однако он легко расщепляется такими донорами, как вода или пиридин, образуя при этом шестикоординационные мономерные комплексы. [13]
Известно, что четырехкоординационные комплексы никеля ( П) в растворах часто находятся в виде двух равновесных форм: тет-раэдрической и квадратной. [14]
Большая скорость реакций с четырехкоординационными комплексами обусловлена, возможно, тем фактом, что в них вокруг центрального иона достаточно места для вхождения в координационную сферу пятой группы. [15]
Страницы: 1 2