Контакт - платина
Cтраница 1
Контакт платины с медными проводниками от потенциометра осуществляется при помощи ртути, наливаемой над впаянной платиновой проволокой почти до верха соответствующих трубок. [1]
С целью поддержания определенного расстояния между электродом и диафрагмой и повышения надежности контакта платины с титановой основой перпендикулярно полоскам платиновой фольги и поверх их с шагом 2 5 см наварены титановые прутки 7 диаметром 2 мм. Ячейка имеет штуцера для ввода и отвода анолита и газоотделительную воронку, прикрытую сверху колоколом для сбора газа, выделяющегося на аноде. [2]
Наиболее существенными недостатками сетчатых анодов являются отсутствие системы охлаждения и коррозия то-кол од водов в месте контакта платины с алюминиевой шиной. Нарушение: контакта приводит к ухудшению распределения тока по поверхности электрода, что ухудшает работу электролизера и требует замены электрода. [3]
Конструкция водородных электродов весьма проста Кусочек платиновой фольги, покрытой тонким слоем платиновой черни, погружают в раствор, через который медленно пропускают водород в области контакта платины с раствором. Фольга запаяна в стеклянную трубку; через нее осуществляется электрический контакт с измерительным прибором. [4]
Платиновый электрод ( рис. 29, а) состоит из платиновой пластинки /, впаянной в стеклянную трубку. Контакт платины с клеммой 4 осуществляется через ртуть 2 и изолированную медную проволоку 3, погруженную в нее. Припой медной проволоки к платине недопустим. [5]
Каломель перед употреблением промывают 2 раза насыщенным раствором хлористого калия для удаления сулемы. Для лучшего контакта платины с ртутью платиновую проволоку электрода перед зарядкой амальгамируют. В сосуд электрода наливают 2 % - ный раствор азотнокислой ртути, слегка подкисленный азотной кислотой, и опускают в него платиновую проволоку, соединенную с положительным полюсом аккумулятора. В течение 3 - 5 мин пропускают ток, затем сосуд электрода хорошо промывают дистиллированной водой и осуществляют зарядку электрода. Во избежание всползания хлористого калия пробку и горлышко сосуда смазывают вазелином. [6]
 |
Схема стандартного водородного электрода при Рн, 101 кПа и ан 1. [7] |
В качестве проводника первого рода для стандартного водородного электрода служит платина. При контакте платины с молекулярным водородом происходит адсорбция водорода на платине. Адсорбированный водород, взаимодействуя с молекулами воды, переходит в раствор в виде ионов, оставляя в платине электроны. При этом платина заряжается отрицательно, а раствор - положительно. Возникает скачок потенциала между платиной и раствором. Наряду с переходом ионов в раствор идет обратный процесс восстановления ионов Н с образованием молекул водорода. Для определения потенциалов электродов по водородной шкале собирают гальванический элемент, одним из электродов которого является измеряемый, а вторым - стандартный водородный электрод. Схему такого элемента записывают следующим образом: слева - водородный электрод, справа - измеряемый электрод. [8]
 |
Схема установки для измерения скорости коррозии металлов рези-стометрическим методом. [9] |
Крепят образец нержавеющей стали к платиновым токоподводам с помощью контактной сварки. Для создания контакта платины с алюминиевыми образцами используют переходную алюминиевую втулку. ТокопоДводы ячейки соединяют с проводами измерительной схемы при помощи посеребренных контактов. [10]
 |
Водородный индикаторный электрод. [11] |
Платинирование ведут в растворе хлорплатината калия с добавкой уксуснокислого свинца. Водород через испытуемый раствор пропускают в области контакта платины с раствором. [12]
В этой заметке речь пойдет не о реакциях, ускоряемых с помощью платины, а о том, как готовятся платиновые катализаторы, в каком физическом состоянии приходят они па химическое илп какое-либо другое производство. Катализатором покрывают развитую поверхность химически инертного носителя - асбеста, пемзы, пористой керамики, кизельгура. Важно при этом, чтобы расход драгоценной платины был поменьше, а поверхность контакта платины с реагирующими веществами - как можно больше. Соблюсти эти противоречивые условия при механическом и даже электрохимическом способе нанесения практически невозможно. Чтобы получить необходимую чистоту и нужное дисперсное состояние катализатора, его в большинстве случаев получают прямо на носителе, восстанавливая соответствующие слои. Асбест замачивают в растворе хлорида платины, а затем муравьинокислого натрия. После выдержки в печи в течение суток при невысокой температуре ( 60 С) получают платинированный асбест, слегка загрязненный поваренной солью и соляной кислотой. Очистка и повторная сушка занимают меньше времени. [13]
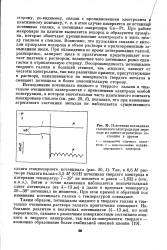 |
Изменение потенциала галлиевогоэлектрода при переходе из одного агрегатного состояния в другое. [14] |
При работе макропары на платине выделяется водород и образуются пузырьки, которые облегчают проникновение электролита в щель меж-ду галлием и стеклом. Возможно, что пульсация связана с вкгхо-дом пузырьков водорода в объем раствора и кратковременный замыканием щели. При охлаждении во время затвердевания галлий, расширяясь, запирает щель и практически предотвращает контакт платины с раствором, вследствие чего потенциал резко сдвигается в отрицательную сторону. Воспроизводимость потенциалов твердого галлия в большей степени, чем жидкого, зависит от чистоты электролита, так как различные примеси, присутствующие в растворе, накапливаются на поверхности твердого металла и смещают потенциал в более положительную сторону. [15]
Страницы: 1 2