Октаэдрическая координация
Cтраница 3
Ввиду особой важности тетраэдрическон и октаэдрической координации мы посвящаем всю гл. Координация по тригоналыюй призме в конечных комплексах встречается очень редко ( примерами могут служить хелаты М ( 52С2К2) з, где М Мо, W, Re, V и Сг, разд. Ег, перечисленные в табл. 3.5); она не характерна п для трехмерных структур, за исключением NiAs, MoS2, A1B2 и родственных структурных типов, а также нескольких ионных кристаллов. [31]
В), находящийся в октаэдрической координации, должен быть меньше. [32]
 |
Линейная, угловая и частотная характеристика группировки Ru-NO. [33] |
Во всех нитрозосоединениях рутений имеет октаэдрическую координацию. Это относится даже к RuNO ( S2CNEt2) 3: если в гр с-диэтилдитиокарбамате Ru ( S2CNEt2) 3 ( реф. NO одна из этих групп становится монодентатным лигандом и уступает одно из координационных мест у рутения нитрозогруппе. [34]
Катион в положении М4 имеет несимметричную октаэдрическую координацию. Четыре координационных атома кислорода ( 05, 05, Ов, О 6) распределены между двумя атомами кремния и, следовательно, заряды их фактически насыщены. При этом два из них ( Ов и Ов) расположены на большом расстоянии от положения М4 и поэтому они довольно слабо влияют на катион, занимающий эту позицию. Четыре других координационных атома кислорода ( 02, 02, 04, 04) связаны только с одним атомом кремния. [35]
Все изученные соединения Си2 с октаэдрической координацией обнаруживают большее или меньшее искажение конфигурации правильного октаэдра. Если в комплексе присутствуют лиганды только одного типа, то комплекс приобретает структуру тетрагональной бипирамиды. Если ион меди связан с двумя типами лигандов, симметрия соответствующего комплекса будет ниже, например, ромбической или моноклинной. [36]
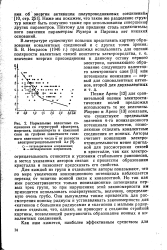 |
Нормальные валентные соединения со структурой сфалерита, вюртцита, халькопирита и каменной соли на графике зависимости главного квантового числа п от разности злектроотрицательностей Д. е. [37] |
О - тетраэдрическая координация; - октаэдрическая координация. [38]
Из табл. 4 видно, что октаэдрическая координация, которая необходима для протекания каталитического акта или адсорбции в том случае, когда одна сторона комплекса занята молекулой пиридина, наиболее выгодна для никелевого комплекса и наименее для медного. Поэтому ряд восприимчивости фталоцианинов к трансвлиянию пиридина на адсорбционные и каталитические свойства может быть объяснен относительной устойчивостью октаэдрической координации для различных центральных атомов металла. [39]
У Со ( П) в октаэдрической координации основным состоянием является 4Tig и можно ожидать большого орбитального вклада в момент. У тетраэдрического Со ( П) основным состоянием является 4Л2 и обычно наблюдаются низкие значения моментов. Но возбужденное триплетное состояние расположено сравнительно близко по энергии и может смешиваться с основным состоянием. [40]
За счет стремления атома металла к октаэдрической координации в этой группе образуются компактные ассоциаты в виде тримера ( ацетилацетонат никеля) или тетрамера ( аце-тилацетонат кобальта), в которых атомы кислорода образуют мостиковые связи, равноценные ковалентным. [41]
Si, где он находится в слабо искаженной октаэдрической координации. [42]
Молекула центросим-метрична, атом германия имеет октаэдрическую координацию, гемопорфиразиновая часть плоская в пределах 0ОЗА. Такое соотношение периметров объясняется наличием более коротких: расстояний С-N 1.274 А в комплексе германия. Можно предположить, что в этом комплексе степень делокализации меньше, чем в молекулах фталоцианинов. [43]
Обычно железо ( II) имеет октаэдрическую координацию. [44]
Атомы железа обычно образуют комплексы с октаэдрической координацией. Что же происходит с двумя координационными положениями выше и ниже плоскости порфиринового цикла. [45]
Страницы: 1 2 3 4