Атом - другой вид
Cтраница 1
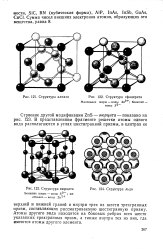 |
Структура алмаза.| Структура сфалерита.| Структура вюрцита Большие шары - ионы S -. маленькие - ионы Zn2.| Структура льда. [1] |
Атомы другого вида находятся на боковых ребрах всех шести указанных трехгранных призм, а также внутри тех из них, где имеются атомы другого элемента. [2]
Атомы одного вида отличаются от атомов других видов весом, размерами и химическими свойствами. [3]
Атомы одного вида отличаются от атомов другого вида массой и свойствами. [4]
Лоренцевское, обусловленное столкновениями с атомами другого вида или атомами посторонних газов. [5]
Очевидно, что совершенно аналогичные уравнения можно написать для числа атомов любого другого вида, входящего в рассматриваемый ряд молекул. [6]
Для силицидов переходных металлов часто характерно окружение атомов одного вида атомами другого вида. Из силицидов 3d -, 4й - переходных металлов можно выделить четыре группы соединений по составу, близких к Me3Si, Me5Si3, MeSi и MeSi2, многие из которых являются фазами переменного состава. Большинство фаз типа Me3Si имеет кубическую решетку, фазы типа Me5Si3 и MeSi2 образуются многими металлами и чаще всего имеют гексагональную и тетрагональную структуры. [7]
 |
Характеристики отдельных элементарных частиц. [8] |
Атомы каждого вида одинаковы между собой, но они отличаются от атомов любого другого вида. Так, атомы углерода, азота и кислорода имеют различные размеры, отличаются по физическим и химическим свойствам. [9]
VA, как показано на рис. 21.3. Каждый атом тетраэдрически окружен четырьмя атомами другого вида. Ребро элементарной кубической ячейки равно 5 40 А, что приводит к длине связи Zn-S 2 34 А, Вюртцит имеет гексагональную структуру, приведент ную на рис. 21.4; она очень близка к структуре сфалерита, соотношение такое же, как между гексагональной и кубической плотнейшими упаковками. [10]
Радиоактивный атом может в результате испускания частиц или f - лучей превратиться в атом другого вида. [11]
В химических процессах электроны могут полностью переходить из электронной оболочки атомов одного вида в оболочку атомов другого вида. При этом образуется ионное соединение. Так, при горении металлического натрия в хлоре атомы натрия отдают по одному электрону атомам хлора. При этом атом натрия создает восьмиэлектронную структуру и, получив положительный заряд, превращается в положительно заряженный ион. [12]
 |
Кристаллическая структура соединений.| Валентные состояния атомов А111 Ву. [13] |
Структура кристаллов Лш Bv аналогична структуре алмаза с той разницей, что центры малых кубов заняты атомами другого вида по сравнению с вершинами и центрами граней большого куба. [14]
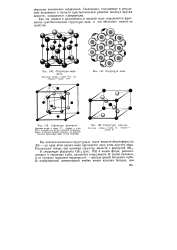 |
Структура вюрт.| Структура флуорита.| Структура рутила. [15] |
Страницы: 1 2 3 4