Кривая - радиальное распределение
Cтраница 1
Кривая радиального распределения дает сведения о межъядерных расстояниях, характере атомного окружения и степени упорядоченности исследуемого объекта. [1]
Кривая радиального распределения, получаемая из данных дифракции электронов, описывает в сущности относительную вероятность нахождения пары атомов на определенном расстоянии. На рис. 3 - 2 показана типичная кривая радиального распределения для 1 2-дихлорэтана. [2]
Кривые радиального распределения атомной плотности для тонкой пленки воды имеют достаточно резкие максимумы и минимумы. С утонь-шением водной пленки происходит некоторое перераспределение в расположении молекул воды. Достаточная резкость максимумов, с увеличением атомной плотности и появление максимумов, соответствующих следующим координационным сферам, указывает на образование на поверхности слюды тонкой пленки воды со структурой, приближающейся к кристаллической. [3]
Кривые радиального распределения электронной плотности для таких катализаторов содержат межатомные расстояния, характерные для г.ц. к, структуры металла, и измененные по площади межатомные расстояния структуры шпинели. [4]
На кривой радиального распределения ПЭ при 145 выявляются три максимума. При введении поправки на смещение максимумов, которое для ПЭ равно 0 42 А, кривая: радиального распределения приходит в хорошее соответствие со схемой гексагональной упаковки. [5]
По кривым радиального распределения атомной плотности широкопористой основы можно предположить, что атомы алюминия большей часты, находятся в тетраэдрнческих пустотах, а октаэдрические пустоты вакантны. [6]
Конечно, кривая радиального распределения - это усредненный результат; но усредняет его эксперимент, а не теория, так как мы всегда имеем дело с макроскопическим образцом, в котором функция распределения обязательно сферически симметрична. И если мы абсолютно точно рассчитаем кривые интенсивности для двух моделей - для полностью беспорядочной сетки и для сетки, в которой упорядоченность флуктуирует в пространстве, - мы не обнаружим никакого различия между кривыми в области обычных углов рассеяния, так как теория в этом случае адекватна эксперименту, усредняющему такие структурные флуктуации. [7]
Иногда на кривой радиального распределения наблюдают не один, а три максимума ( для сплавов алюминий - олово): причем все три максимума можно отнести к первой координационной сфере. Каждый максимум отвечает определенной координации атомов разного сорта: ri 2 70A соответствует расстоянию между атомами алюминия в чистом алюминии, г3 3 40 А - расстоянию между атомами олова в чистом олове. [8]
Из сравнения кривых радиального распределения можно сделать вывод, что положение первого максимума кривой изменяется мало ввиду небольшого различия в положениях его у чистого олова и чистого кадмия. [9]
На всех кривых радиального распределения выявляются внутримолекулярные максимумы в областях 1 45 - 1 50; 2 45 - 2 50 и 3 60 - 3 75 А. Первый максимум, по-видимому, отвечает связи С-С в комплексе со связью С-О. Сложный характер максимума подтверждается расширением максимума до 0 50 А. Второй максимум, по всей вероятности, также является сложным и соответствует расстояниям вдоль цепи между атомами углерода через один атом и между атомамр. Трудно что-либо сказать по поводу третьего максимума из-за его плохой выявлепности. [10]
Общий характер кривых радиального распределения для расплавленных солей и нормальных жидкостей ( металлы и сжиженные благородные газы) одинаков, а это означает, что структура расплавленных солей в принципе аналогична структуре обычных жидкостей. Однако детальное изучение кривых позволяет получить более подробную характеристику строения расплавленных солей. [11]
Это делает кривую радиального распределения мало пригодной для интерпретации. [12]
Донохью [1017] вычислил кривые радиального распределения спиралей полипептидной цепи и определил положения и высоты некоторых пиков. [13]
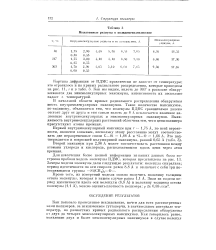 |
Межатомные радиусы в нолидиметилсилоксане. [14] |
В начальной области кривых радиального распределения обнаружены шесть внутримолекулярных максимумов. Такое количество максимумов, по-видимому, объясняется тем, что молекулы ПДМС сравнительно далеко отстоят друг от друга и тем самым вплоть до 8 А исключается взаимное наложение внутримолекулярных и межмолекулярных максимумов. Выяв-ляемость внутримолекулярных расстояний облегчена тем, что в цепи полимера присутствуют атомы кремния. [15]
Страницы: 1 2 3 4