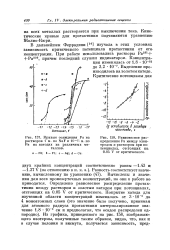
Кинетическая кривая
Cтраница 2
Кинетические кривые для протактиния подчиняются уравнению Жолио-Кюри. [17]
Кинетические кривые, представленные на этом рисунке, построены по экспериментальным данным [92] для реальной сточной жидкости, содержащей смесь прямых и кислотных красителей. [18]
Кинетические кривые для системы, содержащей модификатор, обратимо реагирующий с субстратом. [19]
Кинетические кривые для процесса образования нитрида лития аналогичны кривым автокаталитических реакций: образование нитрида лития вначале идет крайне медленно, затем скорость реакции возрастает, достигая максимального значения, после чего падает до нуля. Реакция взаимодействия лития с азотом относится к типу топохимических реакций. [20]
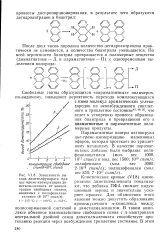 |
Зависимость выхода диметилфумарата при цис-транс-изомеризацни диметилмалеината от концентрации свободных спинов, вводимых с полифенилаце. [21] |
Кинетические кривые (VI.8) изомеризации диметилмалеината показывают, что добавка ПФА снимает индукционный период и значительно ускоряет процесс. [22]
Кинетические кривые для глины ППБ показывают, что степень осветления существенно зависит от концентрации дисперсной фазы. С ростом концентрации скорость оседания уменьшается и соответственно падает степень осветления. [23]
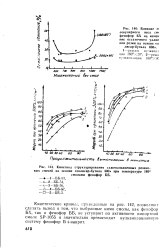
Кинетические кривые, приведенные на рис. 142, позволяют сделать вывод о том, что выбранные нами смолы, как фенофор БХ, так и фенофор ББ, не уступают по активности импортной смоле SP-1055 и значительно превосходят вулканнзационную систему фенофор Б наирит. [25]
Кинетические кривые, полученные при ведении процесса в изотермических условиях в интервале температур 60 - 120 С, отличаются аномальным увеличением скорости или аномальным отклонением от классического уравнения скорости радикальной полимеризации. ММР продукта могут быть рассчитаны иа основании модифицированных уравнений, учитывающих изменение значений кинетических констант с увеличением вязкости среды. [26]
Кинетические кривые, полученные с использованием типично катионных катализаторов - ; комплексов BF3 и SnCl4, имели характерную S-образную форму. Отчетливо наблюдался индукционный период и торможение реакции на неглубоких стадиях превращения мономера. Процесс гет &-рогенный - образующийся полимер нерастворим в любой реакционной среде. [27]
Кинетические кривые, приведенные на рисунке, показывают, что для разрушения эмульсии реагирующих скважин и выделения основной массы воды требуются повышенные расход деэмульгатора и температура нагрева. [28]
Кинетические кривые, выраженные в координатах lg [ - lg ( 1 - п) ] - lg t - это два отрезка с разными углами наклона к оси абсцисс. Независимо от температуры точка пересечения прямых и величина показателя степени г 0 336 для верхней прямой постоянны. Для нижней прямой п составляет 1; 1 6; 1 14; 1 12 для температур 800, 900 и 1000 С, а константа скорости изменяется от 0 0248се - 1 при 800 С до 0 0268 сект1 при 1000 С. Кажущаяся энергия активации, рассчитанная по уравнению ( V. [29]
Кинетические кривые конверсия - продолжительность реакции, полученные в различных условиях, имеют одну общую закономерность. Реакция не идет до конца. Этот эффект принято связывать с гетерогенным характером процесса, поскольку образующийся полимер не растворим в реакционной среде и при кристаллизации из раствора может сорбировать активные центры. [30]
Страницы: 1 2 3 4 5