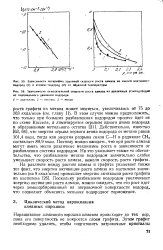
Первый атом - водород
Cтраница 1
Первый атом водорода во всех случаях присоединяется в - положение, а второй - в Р - или б-положение. Таким образом, можно видеть, что при переходе от винилакриловой к сорбиновой кислоте, в которой имеется б-метильная группа, происходит далеко не преимущественное ос б-присоединение, наблюдаемое при наличии б-фенильной группы, на самом деле второй атом водорода присоединяется не только в б -, но частично и в 3-положение. При введении дополнительного ( З - метильного заместителя место присоединения второго атома водорода частично переходит опять к б-положеншо, в то время как введение еще одной б-метильной группы опять вызывает присоединение в р-положепие. [1]
Замещение аммиаком первого атома водорода фосфорной кислоты происходит аналогично нейтрализации азотной кислоты. При замещении второго атома водорода процесс постепенно замедляется, и необходимый избыток аммиака увеличивается в десятки раз по сравнению с замещением первого атома водорода. [2]
Значение энергии отрыва первого атома водорода от молекулы формальдегида может быть оценено на основании данных по фотолизу формальдегида. [3]
 |
Схема реакции гидрогенизации пропадиена в пропен и пропан. [4] |
Можно предположить, что присоединение первого атома водорода происходит по одному из двух путей с образованием двух возможных полугидрированных состояний. Присоединение второго атома водорода дает пропен, который либо адсорбирован на Поверхности, либо непосредственно переходит в газовую фазу. В таком случае относительные изменения количества адсорбированного пропена, подвергающегося десорбции и гидрогенизации, так, как это описано в разделе III, Б, 5 для гидрогенизации ацетилена, будут зависеть от термодинамики и механизма процесса. [5]
В водных растворах Н3Р04 подвергается электролитической диссоциации ступенчато: легко диссоциирует первый атом водорода, заметно труднее - второй и весьма трудно - третий. Уже в первой ступени диссоциации - Н3Р04 Н20 Н30 Н2Р04 - ( Кг 7 - Ю-3) - фосфорная кислота выступает как электролит лишь средней силы. [6]
Действительно, известно 163, 64 ], что энергия отрыва первого атома водорода от метана равна 101 4 ккал, тогда как энергия разрыва связи С - Н в радикале СН2 составляет 89 9 ккал. Поэтому можно ожидать, что при росте алмаза могут иметь место различные механизмы роста в зависимости от разбавления системы водородом. На это указывает также то обстоятельство, что разбавление метана водородом значительно слабее уменьшает скорость роста алмаза, нежели скорость роста графита. [8]
 |
Условное изображение АО иа атомах в молекуле ацетилена. [9] |
Здесь первое слагаемое содержит атомную функцию, отвечающую s - состоянию первого атома водорода, центрированную на этом атоме. Второе слагаемое содержит If-атомную функцию первого атома углерода. [10]
Второй атом водорода отрывается только при очень большом разбавлении, после полного удаления первого атома водорода. [11]
Однако, так же как и в случае с водой, вернее считать, что отрыв первого атома водорода от перекиси водорода должен потребовать затраты большей энергии, чем отрыв второго атома. В табл. 39 приведены значения, предложенные для указанных диссоциаций. Наименее вероятными нужно считать значения, определенные Уолшем [112] на основании чисто теоретических рассуждений. Другие крайние значения для реакции ( 57) даны Эвансом, Хашом и Юр и [115], которые для вывода пользовались интересной методикой; к сожалению, мы не можем здесь на ней остановиться. Робертсон [114] методом электронной бомбардировки определил верхний предел теплоты реакции ( 57); он равен 90 ккал. Таким образом, окончательная величина для теплоты реакции ( 57) не известна; мы примем для этой теплоты значение 90 ккал / моль, следовательно, значение для реакции ( 58) оказывается равным 46 ккал / моль. Езыло бы весьма желательно поставить дополнительные опыты для более точного определения необходимых значений. [12]
Задача определения, например, того, все ли атомы железного катализатора синтеза аммиака способны связывать с одинаковой силой первый атом водорода, приближающийся к поверхности, чрезвычайно трудна. В прошлом считалось [73], что если малое количество яда способно дезактивировать некоторые катализаторы, то это является доказательством активности только части центров поверхности. Однако другие количественные исследования [80] по отравлению поверхностей металлов указывают на их однородность. Де Бур [78] и Уилер [81] считают, что сильное действие некоторых ядов может быть обусловлено тем, что они блокируют значительную часть поверхности, располагаясь в устьях пор катализатора. [13]
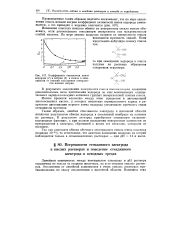 |
Коэффициент активности ионов / Si-UNa. [14] |
Можно провести аналогию между этим процессом и диссоциацией многоосновных кислот, у которых появление отрицательного заряда в результате диссоциации первого атома водорода увеличивает прочность связи оставшихся протонов. [15]
Страницы: 1 2 3 4