Кристалл - гидрат
Cтраница 3
Аргон также соосаждается с гидратом двуокиси серы и распределение его между газовой фазой и кристаллами происходит по закону Бертло - Нернста, если кристаллы гидрата успевают многократно перекристаллизоваться. Этим методом можно количественно перевести в осадок аргон, несмотря на то, что упругость диссоциации его гидрата при такой температуре достигает десятков атмосфер. [31]
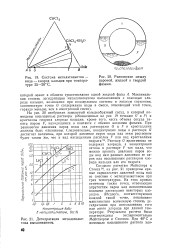
На рис. 20 изображен замкнутый кольцеобразный сосуд, в который помещены насыщенные растворы ( обозначенные на рис. 19 точками G и F) и кристаллы гидрата хлорида кальция; кроме того, часть объема сосуда занята паром V, находящимся в контакте с обеими жидкими фазами. При равновесии давления паров воды над растворами G и F и кристаллами должны быть одинаковы. [33]
При изучении гидролиза и гидратации трехкальциевого силиката установлено, что если реакция происходит при температуре 150, то получаются хорошо образованные кристаллы гидрата двухкальциевого силиката и кристаллы гидрата окиси кальция. При твердении портландцементов в условиях автоклавной обработки или длительного твердения также наблюдается образование кристаллических гидросиликатов кальция. [34]
В период 1928 - 1938 гг. Брэдли, Колвин, Коппер, Юм, Смит и Топли опубликовали ряд статей, в которых рассматривалась скорость продвижения поверхности дегидратации в кристаллах гидратов солей, имеющих определенную форму и размеры. [35]
В проведенных нами исследованиях при испарении растворов силикатов калия ( 20 масс. % SiC2, 2 5 - 3 5) было обнаружено образование очень мало растворимых и практически не разлагающихся водой кристаллов гидрата тетрасиликата калия K. [36]
Если через охлажденную до О С воду пропускать некоторые газы ( Аг, Кг, Хе, Cl2, Brz, ШО, РНз, SO2, Ш5, СНд и др.), то выделяются кристаллы гидратов газов, состоящие из полиэдров, включающих до 20 и больше молекул воды, связанных между собой водородными связями и занимающих вершины полиэдра. Внутри полости таких полиэдров находятся молекулы газов. Размер полости ( клетки) колеблется от 400 до 750 пм. Получены зеленовато-желтые кристаллы С1зф ( 7 лг) Н2О, устойчивые на воздухе ниже 9 С; желтоватые кристаллы СЮ2 ( 6 дс) Н2О, с температурой разложения 15 С; бесцветные кристаллы 8О2ф ( 6 лс) Н2О, устойчивые ниже 7 С. [37]
Степень заполнения каркаса молекулами гидратообразующих газов определяется для данного состава газа в основном давлением и температурой системы. Кристаллы гидратов зарождаются на поверхности раздела фаз системы газ-вода. Свободная вода после образования гидратов продолжает переходить в гидратное состояние только при перемешивании фаз и при наличии соответствующих термодинамических условий. При отсутствии необходимой степени перемешивания диффузия газа через твердую пленку гидрата становится затруднительной и дальнейший рост гидратов прекращается. [38]
Гидрат свободен от соли. Кристаллы гидрата отделяют, фильтруют, промывают пресной водой ( - 10 вее. [39]
Форма кристаллов гидратов алюминия до 1373 К не изменяется, несмотря на протекающие полиморфные превращения. [40]
В нескольких опытах к аргону был примешан воздух. В кристаллах гидрата двуокиси серы были тогда обнаружены и азот и кислород, хотя в несколько меньших количествах, чем аргон. Таким образом, самый факт существования гидратов этих газов можно считать доказанным. В этих опытах кристаллы представляли собою изоморфную смесь, по меньшей мере четырех гидратов - двуокиси серы, аргона, азота и кислорода. [41]
В зависимости от термодинамических условий роста кристаллогидраты углеводородов имеют разнообразную форму. В статике кристаллы гидрата метана и этана принимают лучевидную форму, гидраты пропана и бутана образуют колонии нитевидных, слегка изогнутых или резко ломанных кристаллов. При высокой турбулентности потока гидраты формируются в виде аморфных накоплений. [42]
В каждом впуске аргон распределяется между газовой фазой и кристаллами гидрата по закону Бертло-Нернста. Очевидно, свежевыпавшие кристаллы гидрата SO, настолько малы, что скорость их перекристаллизации очень велика. Напомним здесь, что при быстрой кристаллизации из пересыщенных растворов соосаждение тоже происходит по закону Бертло - Нернста. Хлопин и его сотрудники [39] объясняют это явление тем, что первоначально из пересыщенного раствора выпадают субмикроскопические кристаллики, успевающие многократно перекристаллизоваться в очень короткий срок. [43]
После этого выделяющийся хлор пропускают в пробирку с водой, погруженную в охладительную смесь воды со льдом; следят за тем, чтобы воду не засасывало в трубку. Наблюдают появление кристаллов гидрата хлора С12 - 6Н2О, которые начинают быстро плавиться при нагревании пробирки рукой. Расплавляют кристаллы и приливают к раствору четыреххлористый углерод, который растворяет хлор лучше, чем вода; встряхивают пробирку и сравнивают окраску водного слоя и слоя четыреххлористого углерода. [44]
Для более полного отделения кристаллов гидрата от маточного рассола пользуются следующими методами: 1) дренирование через гидраты с последующей отмывкой кристаллов пресной водой, которая образовалась в результате плавления части кристаллов; 2) центрифугирование гадратной массы; 3) выжимание рассола из гидратной массы в процессе прессования. Процесс очистки кристаллов гидрата при центрифугировании можно улучшить, добавляя к рассолу поверхностно-активные вещества. Так, при добавке сульфанола отмывка гадратных кристаллов происходит полнее. [45]
Страницы: 1 2 3 4