Белковый кристалл
Cтраница 2
Выпускается промышленностью в виде светло-серого порошка, состоящего из спор бактерии, токсических белковых кристаллов и инертного наполнителя. [16]
Пепсин - однокомпонентный про-теолитический фермент желудочного сока - может быть получен в виде белковых кристаллов, обладающих весьма высокой каталитической активностью. Пепсин является альбумином, имеет глобулярные молекулы и растворим в воде. Пепсин свертывается при нагревании, осаждается крепким спиртом, солями тяжелых металлов, дубильными веществами. Концентрированные кислоты и щелочи разрушают пепсин. Фильтровальная бумага адсорбирует значительные количества пепсина. Свет способствует инактивации фермента. [17]
 |
Гусеницы капустной моли, погибшие после опрыскивания растения суспензией энтобактерина. [18] |
Выпускается промышленностью в виде светло-серогс смачивающегося порошка, состоящего из спор бактерии, токсических белковых кристаллов и инертного наполнителя - тонко размолотого каолина. [19]
Заметим, что в настоящее время проблема многоволнового рассеяния становится более актуальной в связи с исследованием структуры белковых кристаллов. Это связано с соотношением длин волн используемого рентгеновского излучения и периодов решеток подобных структур. [20]
Следует заметить, что связи, определяющие конформацию молекулы белка, являются внутримолекулярными и, в первом приближении, не зависят от характера среды. Таким образом рентгеноструктурный анализ белковых кристаллов позволяет детально определять те конформации молекулы, которые идентичны ( или почти идентичны) конформациям, характерным для биологических систем. Хотя другие методы позволяют изучать молекулы в условиях, более близких к нативным, рентгеноструктурный анализ дает несравненно более подробную информацию, чем любой из них. [21]
Приведенные выше данные показывают, что при гидратации белковых кристаллов и растворенных белков наибольшее сокращение объема наблюдается в области низкого давления водяного пара ( см. фиг. Кажущийся удельный объем белйов в белковых кристаллах вряд ли отличается от кажущегося удельного объема белков в растворе. Обе эти величины, однако, значительно ниже величин удельного объема сухих белков. [22]
Более существенные работы исходят из представлений о фазовых переходах в мышце. Сокращение мышцы происходит в результате плавления белковых кристаллов. Активной фазой является релаксация, а не сокращение. Роль сократительного белка состоит в сопротивлении сжатию, роль АТФ - в воздействии на предполагаемый фазовый переход. [23]
Пятна интерференции, полученные в этих первых анализах, обусловлены периодичностью аминокислотных остатков вдоль пептидной цепочки [61] или периодичностью в расстояниях между параллельными пептидными цепочками внутри белковой молекулы. Очевидно, что этот метод не может дать каких-либо сведений о действительных размерах первичных ячеек в белковых кристаллах. [24]
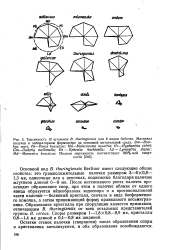
Berliner имеет следующие общие свойства: это грамположительные палочки размером 3 - 6X0 8 - 1 3 мк, одиночные или в цепочках, подвижные благодаря наличию жгутиков длиной 6 - 8 мк. После интенсивного роста палочек происходит образование спор, при этом в палочке вблизи от одного конца образуется яйцеобразная эндоспора и в противоположной части палочки - белковый кристалл, сначала в виде бесформенного комочка, а затем принимающий форму правильного восьмигранника. Образование кристалла при споруляции является признаком, отличающим В. Споры размером 1 - 1 8x0 8 - 0 9 мк, кристаллы 0 8 - 1 4 мк длиной и 0 4 - 0 8 мк шириной. [26]
Но почему авторы не приводят картины белкового кристалла. Белковые кристаллы являются кристаллами совершенно необычными. Это делает их съемку в электронном микроскопе невозможной. [27]
Сравнивая левые и правые стороны рис. 42 и 43, мы легко находим пятна с положительными и отрицательными знаками амплитудных коэффициентов. В этом и заключена, правда с большими упрощениями, основная физическая идея метода изоморфного замещения. При анализе белковых кристаллов дело обстоит несравненно сложнее. Но в принципе брэгговская иллюстрация помогает понять идеи метода. [28]
Замечательным свойством белкового кристалла является то, что молекулы, из которых он построен, соприкасаются друг с другом лишь незначительной частью своей поверхности. Большая же часть межмолекулярного пространства заполнена водой. При осторожном высушивании белкового кристалла он терпит превращения, меняющие взаимное расположение молекул. Большую часть воды можно удалить, сохранив кристалличность белка. [29]
Страницы: 1 2 3 4