Вторичный атом - водород
Cтраница 1
Вторичный атом водорода мигрирует быстрее, чем первичный. Наличие двойной связи в а р - или р у-положениях затрудняет перегруппировку. Окси-кетоны перегруппировываются с трудом. [1]
При этом вторичный атом водорода замещается хлором легче, чем первичный. Наличие гало-геппих ааместитслей затрудняет дальнейшее га доге встревание и притом особенно сильно у атома углерода, ужо имеющего галогеа. Но мере удаления от этого атома влияние галогенного заместителя ослабляется. Наличие двух или трех атомов хлора у одного и того же атома углерода препятствует дальнейшему свобо дно ра дика лъ-поьгу хлорирован то ЗОЙСГ2 таких соединений, как, например, хлороформ, тетра-хлорэтан или хлористый бензшшден. [2]
В данном случае замещению подвергается вторичный атом водорода, который активирован соседним бензольным кольцом. Воздух продувают в горячий углеводород при 70 С до тех пор, пока около 10 % его не превратится в гидроперекись. При перемешивании с раствором едкого натра гидроперекись распадается а а-тетралон и воду. Смесь высушивают и фракционируют, регенерируя большую часть углеводорода. [3]
Удельный вес, который занимают вторичные атомы водорода в молекуле парафина, увеличивается с длиной цепи. [4]
При окислении пропана в первую очередь реагирует вторичный атом водорода. В этом случае оптимальное соотношение равно 2 объемным частям пропана, 2 объемным частям кислорода и 1 объемной части бромистого водорода; время пребывания в зоне реакции составляет около 3 мин. [5]
Аналогичным путем легко можно понять, почему вторичный атом водорода замещается труднее третичного, но легче первичного. [6]
Широко известна химикам-органикам большая подвижность в парафиновых углеводородах третичных и вторичных атомов водорода по сравнению с первичными. Но сравнительно мало кто помнит, что и это правило впервые и четко было сформулировано Марковниковым: в предельных углеводородах водороды, принадлежащие углеводородным паям, наиболее потратившим свои сродства на связь с другими углеводородами, легче подвергаются замещению сравнительно с другими ( стр. Коновалова, в работах С. С. Наметкина, в советское время в исследованиях П. П. Шорыгина и А. В. Топчиева, В. В. Тронова, А. И. Титова), сульфирования ( в работах А. П. Терентье-ва, В. В. Козлова и др.), алкилирования ( исследования школы Н. Д. Зелинского) и ряде других реакций. [7]
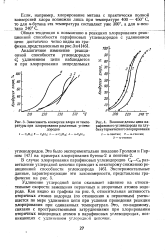 |
Зависимость конверсии хлора от темпе. [8] |
Удлинение углеродной цепи оказывает влияние на относительные скорости замещения первичных и вторичных атомов водорода. Как видно из графика на рис. 6, относительная активность вторичных атомов водорода ( по отношению к первичным) уменьшается по мере удлинения цепи при условии проведения реакции хлорирования при одинаковых температурах. Это, по-видимому, связано с пространственными затруднениями при хлорировании вторичных водородных атомов в парафиновых углеводородах, возникающих с удлинением углеродной цепочки. [9]
Наблюдаемая закономерность объясняется тем, что с ростом длины углеродной цепочки увеличивается количество реакционно-способных вторичных атомов водорода. [10]
Отсюда вытекает, что первичный атом водорода метильной группы реагирует при дегидрохлорировании более вяло, чем вторичный атом водорода метиленовой группы. Если, напротив, соединенный с галоидом атом углерода находится между двумя метиленовыми группами ( - СН2СНС1СН2 -), то при прочих равных условиях олефин может образоваться легче, чем при группировке - СЕЬСНСЮНз. В первом случае галоид находит у соседних атомов углерода равноценные по реакционной способности атомы водорода метиленовых групп; во втором случае хотя и имеется больше атомов водорода, которые могут отщепиться, но из них первичные атомы менее активны. [11]
Следовательно, если принять относительную скорость замещения первичного атома водорода метальной группы за единицу, то вторичный атом водорода метиленовой группы реагирует в 3 25 раза, а третичный атом водорода метановой группы в 4 43 раза быстрее. [12]
Показано [191, 193-195], что строение моносульфохлоридов может быть определено по правилу Хасса [ 192J, согласно которому замещение вторичного атома водорода происходит примерно в 3 25 раза быстрее, чем первичного. [13]
В полтора раза большее значение Фц2 для изопропанола вполне объяснимо, потому что в нем значительно ослаблена связь вторичного атома водорода. Это приводит к легкому отрыву атома водорода в первичном процессе. Другие продукты согласуются с этим механизмом, если принять во внимание вторичные реакции атомов Hg ( sPi) с продуктами. [14]
Во-первых, в разветвленной молекуле метильпые группы стремится расположиться на периферии, третичные водородные атомы - спрятаться внутрь молекулы, а вторичные атомы водорода занимают промежуточное положение. Вследствие этого объемистый радикал с трудом может атаковать слабо связанный третичный атом водорода, в то время как легче доступные вторичные и первичные атомы водорода связаны более прочно. [15]
Страницы: 1 2 3 4