Кислородный атом - группа
Cтраница 1
Кислородные атомы групп СО3 в элементарной ячейке расположены в вершинах треугольника, плоскость которого перпендикулярна тройной оси. Расстояние С-О равно - 1 24 - 10 - 4 мкм. Каждая группа СОз окружена шестью атомами Са. Кристаллы кальцита имеют совершенную спайность по трем направлениям. [1]
Димерная молекула галогенида координируется с кислородным атомом группы OR с последующим формированием переходного циклического активного комплекса за счет передачи электронов атомом галогена наиболее электрофильному центру. Таким центром, в зависимости от сравнительной полярности связей Si - О и С - О, может быть и атом кремни. [2]
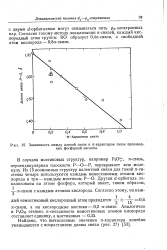 |
Зависимость между длиной связи и it - характером связи производи. [3] |
Согласно такому методу локализации я-связей, каждый кислородный атом группы RO образует 0 4л - связи, а свободный атом кислорода - 0 8я - связи. [4]
Соединение III в этих условиях не лактонязуется; по правилу Марковникова присоединение карбоксильной группы должно осуществляться в р-положение с образованием р-бутиролактона, но кислородный атом группы СОО - не может приблизиться к центру лактонизации из-за того, что углы в цикле должны стать много-меньше тетраэдрических. [5]
В одной из теорий ориентации замещения ароматических соединений, основанной на концепции Вернера о частичном расходовании химического сродства ( Флюршейм, 1902 г.), принималось, что некоторые атомы, как, например, пятивалентный атом азота К02 - группы, расходующий все свое сродство на соединение с атомами кислорода, развивает слабое сродство по отношению к углероду, тогда как, например, кислородный атом фенолыюй группы, связанный одной из своих валентностей с водородом, сильно влияет на атом углерода, с которым он связан второй валентностью. Таким образом, атом углерода ароматического ядра может быть связан со своим заместителем либо связью с большим сродством, либо связью с малым сродством. В нервом случае атомы в орто-пара-положениях обладают большим остаточным сродством ( изображенным длинными пунктирными линиями) и, следовательно, они более реакционпоспособны; во втором случае повышенной реакционной способностью характеризуются лета-положения. [6]
Кальцит кристаллизуется в гексагональной системе, плотность его 2600 - 2800 кг / м3, твердость 3 по шкале Мооса. Кислородные атомы группы СО3 в элементарной ячейке расположены в вершинах треугольника, плоскость которого перпендикулярна тройной оси. Расстояние О-О равно 0 124 10 - нм. Каждая группа СОз окружена шестью атомами кальция. [7]
Реакции замещения производных N-окиси пиридина будут рассмотрены ниже. Как видно из предельных структур IX-XII, кислородный атом N-окисной группы может выступать в качестве нуклеофильного реагента. Это свойство было обнаружено при изучении реакций производных N-окиси пиридина с различными алкилирующими агентами. [8]
Реакции замещения производных N-окиси пиридина будут рассмотрены ниже. Как видно из предельных структур IX-XII, кислородный атом N-окисной группы может выступать в качестве нуклеофильного реагента. Это свойство было обнаружено при изучении реакций производных N-окиси пиридина с различными алкилирующими агентами. В результате этих реакций, протекающих по 5 2-механизму, образуются соли N-алкоксипиридиния. [9]
Приведенные в табл. III-2 константы таутомерного равновесия получены различными авторами, в разных условиях и разными методами, что несколько затрудняет сравнение, однако видна четкая тенденция. Как и в случае хлорангидридов, нуклео-фильный центр ( кислородный атом группы - СООН) должен приблизиться почти перпендикулярно к плоскости карбонильной группы для того, чтобы могла осуществиться циклизация. [10]
На ориентацию при реакции нитрования особенно большое влияние оказывает стабильность переходного сг-комплекса. Например, возможность дополнительной стабилизации ст-комплекса за счет взаимодействия с кислородным атомом орто-расположенных групп - СНО, - СООН, - NO2, - SO3H приводит к образованию в значительных количествах орто-нитроизомеров, несмотря на то, что, перечисленные группы имеют электроноакцепторный характер. [11]
Интересно отметить, что ИК-спектры экстрактов V ( III) и V ( IV) идентичны. Это обстоятельство также подтверждает мнение, высказанное в литературе [1], о том, что строение тройных комплексов зависит от характера взаимодействия отдельных элементов с кислородом карбонильных групп, а уменьшение или увеличение ковалентности образующейся донорно-акцепторной связи влияет на прочность соединений. Как известно, ионы трех-и четырехвалентного ванадия отличаются склонностью к образе-ванию координационной связи через кислородные атомы групп адденда. [12]
Учитывая, что в условиях восстановления алкоксиборогидриды натрия не диспропорционируют ( однозначно это удалось показать лишь для моноалкоксиборогидрида натрия), следует признать, что реакция последовательного восстановления карбонильного соединения осуществляется четырьмя разными восстанавливающими агентами. В результате реакции образуется свободный спирт и тетраалкоксибораты, имеющие алкоксигруппы растворителя. Роль растворителя, однако, этим не ограничивается. По-видимому, он выполняет одновременно функцию электрофиль-ного катализатора, координируясь с кислородным атомом группы СО. [13]
Возможно, что бидентатная координация не является предпочтительным способом взаимодействия ионов металлов с производным фосфатов в бинарных комплексах. Действительно, если напряжение в кольцевой структуре бидентатного комплекса велико, то можно ожидать, что он будет неустойчив по сравнению с монодентатным комплексом. Активация в тройном комплексе фермент-металл - субстрат может быть результатом сдвига в сторону бидентатной координации фосфатной группы вследствие стерического влияния активного центра. Для бидентатной активации переноса фосфата от АТФ необходимо присоединение металла к двум кислородным атомам концевой фосфатной группы. Аналогично этому для бидентатной активации переноса нуклеотидной группы необходима координация с двумя кислородными атомами а-фосфатной группы. Хотя любая из этих структур гораздо менее выгодна по сравнению с шестичленными кольцевыми структурами, под влиянием подходящего фермента они могут стабилизироваться. [14]
Страницы: 1