Кристаллизант
Cтраница 1
Кристаллизант и примесь сорбируются в основном гранями оснований кристалла. Различные участки этих граней по-разному омываются раствором. Участки грани, прилегающие к ребру кристалла, на которое набегает раствор, омываются жидкостью лучше, чем центр граней. Это связано с тем, что скорость движения раствора у ребра кристалла равна i 0, а в центре грани она уменьшена из-за тормозящего влияния адсорбционного слоя. В результате этого массоперенос к ребру происходит интенсивнее, чем к центру грани. Если совместить одну из координатных плоскостей с гранью основания кристалла, а одну из осей координат - с ребром, на которое набегает раствор, то при достаточно протяженных ( полубесконечных) гранях массоперенос к любой точке границы раздела фаз будет зависеть в основном от удаленности этой точки от ребра, совмещенного с осью координат. [1]
Если комплексообразование кристаллизанта незначительно ( n i 0), а примесь и кристаллизант не взаимодействуют в материнской фазе ( pi 0), то при переходе примеси в междоузлия решетки кристаллов ( ге - 0), и при образовании каждой ( i 1) - формы примеси. [2]
При малой растворимости кристаллизанта и D3 1 метод сокристаллизации более точен, чем другие способы определения растворимости. [3]
Рассмотрим вначале влияние кристаллизанта, приняв концентрации введенных комплексообразователей и коэффициенты термодинамической активности всех форм постоянными. [4]
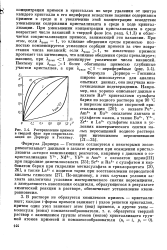 |
Распределение примеси в твердой фазе при сокристалли-зации по Дорнеру и Госкинсу. [5] |
При уменьшении концентрации кристаллизанта в среде возрастает число вакансий в твердой фазе ( см. разд. При этом, если А равн 1, то влияние обеднения среды примесью полностью компенсируется усилением сорбции примеси за счет возрастания числа вакансий; если Яравн 1, то извлечение примеси протекает так интенсивно, что влияние обеднения среды превалирует; наконец, при Ярпрн 1 доминирует увеличение числа вакансий. [6]
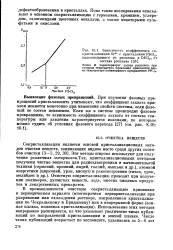 |
Зависимость коэффициента со. [7] |
При изучении фазовых превращений кристаллизанта учитывают, что коэффициент захвата примеси меняется монотонно при изменении свойств системы, если фазовый ее состав неизменен. [8]
А у - масса кристаллизанта, вводимая в систему в единицу времени. [9]
Рассмотрены методы обратимого изменения состава кристаллизанта, высаливания, экстрактивной кристаллизации, образования соединений включения, многоступенчатой кристаллизации, зонной сублимации, фракционированной десублима-ции, непрерывной противоточной сублимации и реакционной сублимации. Показаны вреимущества и недостатки каждого метода. [10]
В течение периода т молекулы кристаллизанта и примеси могут переходить на участок FJ непосредственно с торца ступени, заполняя вакансии в этом объеме. [11]
Таким образом, потоку молекул кристаллизанта на молекулярно-гладкую поверхность сопутствует почти равный ему противоток. Однако точечная дефектность этих участков значительно превышает равновесную даже при малых пересыщениях, так что кристаллу приходится ликвидировать неравновесную разупорядоченность позднее. [12]
Скв и С - концентрации кристаллизанта в вводимом растворе и в растворе, из которого происходит сокристаллизация. [13]
Эти изотермы показывают зависимость количества выделившегося кристаллизанта х ( моль / м2) от метастабильной концентрации Ср, установившейся после завершения первой стадии кристаллизации. [14]
Предположим, что разреженный молекулярный пар кристаллизанта и примеси находится в равновесии с кристаллами, в объеме которых можно выделить молекулы, связанные значительно слабее, чем атомы внутри молекул. [15]
Страницы: 1 2 3 4