Кристаллик - железо
Cтраница 1
Кристаллик железа - - кубический; измерим основное межплоскостное расстояние для системы плоскостей, параллельных грани куба. Опыт дает цифру 1 4 А. Посчитаем, сколько атомов железа приходится на кубик с ребром 1 4 А. На кубик объемом ( 1 4) 8 - 10 - 24см3 приходится масса ( 1 4) 3 - 10 - 24 - 7 88 21 7 - 10 - 24 г. Но это число в четыре раза меньше массы атома железа. Значит, элементарная ячейка железа имеет ребро больше 1 4 А. [1]
Кристаллик железа - кубический; измерим основное межплоскостное расстояние для системы плоскостей, параллельных грани куба. Опыт дает цифру 1 4 А. Посчитаем, сколько атомов железа приходится на кубик с ребром 1 4 А. [2]
Сталь состоит главным образом из мельчайших кристалликов железа, смешанных с зернами карбида железа, - так называемого цементита Fe3C и углерода. При соприкосновении с электролитом на поверхности стали образуется множество микрогальванических элементов, в которых анод - железо, катод - цементит или углерод. При работе таких гальванических элементов электроны перемещаются от Fe к Fe3C или к С, затем к кислороду или ионам водорода, а атомы железа превращаются в ионы. В результате железо разрушается. [3]
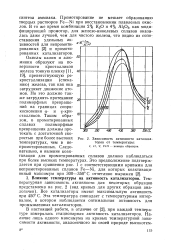 |
Зависимость активности катализаторов от температуры. I, II, V, VIII - номера образцов. [4] |
Окислы калия и алюминия образуют на поверхности кристалликов железа тонкую пленку [11, 40 19], препятствующую рекристаллизации ( спеканию) железа, так как она затрудняет движение атомов. Но это должно также затруднять протекание полиморфных превращений на границах соприкосновения х - и у-кри-сталликов. Таким образом, в промотированных сплавах полиморфные превращения должны протекать с достаточной скоростью при более высоких температурах, чем в не-промотированных. [5]
Так, при промотировании железного катализатора для синтеза аммиака окисью алюминия создается на поверхности кристалликов железа сетчатая пленка, препятствующая рекристаллизации. [6]
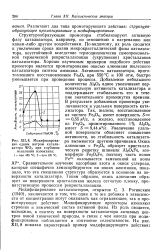 |
Модифицирова - ра вызывается другими причинами. Окись. [7] |
Сравнительное изучение адсорбции азота и окиси углерода, которые специфично хемосорбируются на ионах алюминия, показало, что эта смешанная структура образуется в основном на поверхности катализатора. Таким образом, окись алюминия образует на поверхности кристалликов железа сетчатую пленку, препятствующую процессам рекристаллизации. [8]
Ориентирующее поле поверхностных частиц исходной фазы сильно понижает энергию образования зародышей новых фаз. Действительно, соблюдение принципа ориентационно-размеряого соответствия отмечалось для этих превращений выше. Например, известно [185], что возникающие при распаде FeO кристаллики железа ориентированы по отношению к исходным. Они образуются на определенных кристаллографических плоскостях FeO. [9]
Однако высказывалось мнение, что поляризация при электроосаждении, например, никеля не может быть полностью сведена к замедленности стадии разряда [173, 174], а в зависимости от условий частично связана и с трудностью образования и роста зародышей. Так, недавно было показано [175], что на пассивной поверхности образование зародышей железа является самой медленной стадией и требует перенапряжения свыше 1 5 в. Было исследовано электролитическое выделение кристаллических зародышей железа на пассивном платиновом сферическом монокристалле из буферного раствора: 1 5 Л7 FeSC4 1 Л АЬ ( 804) 3 - Метод заключался в наложении импульсов напряжения от 1 5 до 2 4 в, длительностью от 20 до 40 мсек, в последующем проявлении образовавшихся во время импульса зародышей путем наложения малой катодной поляризации и подсчете получившихся кристалликов железа. [10]
В гальванической паре Fe - Sn анодом будет уже железо, которое и разрушается ( рис. 107, б), а катодом - олово. Следовательно, олово защищает железо от коррозии до тех пор, пока оно обеспечивает сплошное его покрытие. Подобные же явления происходят и тогда, когда в металле, находящемся в электролите, будут находиться примеси других металлов. В этом случае на поверхности металла и в его трещинах возникает множество микрогальванических элементов, в которых примеси обычно представляют собой катоды, а кристаллики самого металла аноды. В стали находятся кристаллики железа, карбида железа Fe3C и углерода. В электролите разрушается железо. [11]
По-видимому, их роль сводится к увеличению срока жизни микрокристаллической фазы катализатора, неустойчивой вследствие термодинамически самопроизвольной термической рекриста лл. Хорошо изученным примером подобного действия промотора является промотиррвание окисью алюминия железного катализатора синтеза аммиака. Активность катализатора, приготовленного восстановлением Fe3O4 при 550 С и 100 агЗИ, быстро уменьшается при проведении процесса. Добавление небольшого количества А12О3 вдвое увеличивает первоначальную активность катализатора и поддерживает стабильность его в течение значительного промежутка времени. В результате добавления промотора увеличивается и удельная поверхность катализатора. Так, железо, восстановленное из чистого Fe3O4, имеет поверхность 5 0 55 м2 / г, а железо, восстановленное из Fe3O i, промотированного 1 % А12О3, имеет S 9 44 м2 / г. Увеличение удельной поверхности объясняет повышение активности, но стабильность катализатора вызывается другими причинами. Сравнительное изучение адсорбции азота и окиси углерода, которые специфично хемосорбируются на ионах алюминия, показало, что эта смешанная структура образуется в основном на поверхности катализатора. Таким образом, окись алюминия образует на поверхности кристалликов железа сетчатую пленку, препятствующую процессам рекристаллизации. [12]
Страницы: 1