Кристиансен
Cтраница 1
 |
Многоэлементный интерферометр крестообразного типа. [1] |
Кристиансен и Уорбартон [62] разработали многоэлементный интерферометр для частоты 1420 Мгц. [2]
Кристиансен и Ледерер [27] исследовали растворы соединений родия ( Ш) в 6 N НС1 спектрофотометрическим и хроматографиче-ским методами. Состояние равновесия достигается при 110 С приблизительно через час. [3]
Дейл и Кристиансен [39, 40] синтезировали 15-краун - 5 ( выход 20 %), 18-краун-б ( выход 33 %) и 21-краун - 7 ( выход 26 %) добавлением растворов диола и дито-зилата в бензоле к суспензии ярея-бутилата калия в горячем бензоле без использования техники высокого разбавления. [4]
Дейл и Кристиансен [39, 40] синтезировали 15-краун - 5 ( выход 20 %), 18-кра-ун - 6 ( выход 33 %) и 21-краун - 7 ( выход 26 %) добавлением растворов диола и дито-зилата в бензоле к суспензии ярея-бутилата калия в горячем бензоле без использования техники высокого разбавления. [5]
Петтиджон и Кристиансен [42] в обширном экспериментальном исследовании влияния формы частицы на скорости свободного падения нескольких изометрических частиц заключили, что сферичность i) является подходящим параметром для описания среднего сопротивления таких частиц. [6]
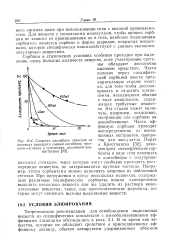 |
Скорость адсорбции трипсина на частицах препарата соевый ингибитор трипсина-агароза в суспензиях, различной концентрации. [7] |
Порат и Кристиансен [32] рекомендуют специфические сорбенты в виде геля помещать в контейнеры с полупроницаемыми стенками, через которые могут свободно проходить растворенные вещества, но задерживаются крупные частицы. [8]
Сивин и Кристиансен [132] вывели соотношения, подобные уравнениям ( VI. [9]
Для нахождения оптимальных условий Порат и Кристиансен [32] рекомендуют предварительными экспериментами определить емкость колонки. Это определение лучше всего может быть осуществлено фронтальной хроматографией на колонке с общим объемом в несколько миллилитров. [10]
Те резерфордояские работы были знакомы Бору со студенческих лет: Кристиансен однажды поручил ему сделать обзорный доклад о радиоактивных семействах. [11]
Например, Вебер [ 57 ( 6) ] сначала титрует железо с сульфосалициловой кислотой, а затем определяет содержание А1 при рН 5 обратным титрованием избытка НТА раетворо м соли меди с Биндшедлера зеленым. Кристиансен [ 61 ( 44) ] сначала определяет железо при рН 2 с З - окси-2 - нафтойной кислотой в растворе, охлаждаемом внесением кусочков льда. После того как достигается точка эквивалентности титрования Fe ( переход синей окраски в желтую), раствор нагревают до 50 С, повышают рН до 3 и титруют А1 с тем же индикатором в УФ-лучах до перехода синей флуоресценции в зеленую. По отношению к А1 маскирующее действие оказывает сульфосалициловая кислота. Допускаются большие количества А1, если сначала определить содержание Fe при рН 1 - 2 с алюминоном, затем повысить рН раствора до 4 4 и титровать А1 с тем же индикатором. [12]
Особенное значение в аналитической практике имеет часто встречающееся в различных комбинациях определение Fe и А1 в их смеси. Это возможно в том случае, если присутствует вспомогательное комплексообразующее вещество и подобраны определенные индикаторы. Вспомогательное комплексообразующее вещество может одновременно служить индикатором. Например, Бегельфер [ 62 ( 13) ] сообщает, что в присутствии большого количества сульфосалициловой кислоты можно сначала оттитровать Fe при рН 2 - 3, затем прибавить ЭДТА, повысить рН до значения 4 - 4 5, прокипятить раствор и после охлаждения обратно оттитровать избыток ЭДТА стандартным раствором соли железа. Вебер [ 57 ( 6) ] вначале титрует Fe с сульфосалициловой кислотой, а затем определяет AI обратным титрованием избытка НТА раствором меди с Биндшедлера зеленым. Согласно Вакамацу [ 60 ( 169) ], можно определять Fe с сульфосалициловой кислотой, а А1 - обратным титрованием ЭДТА раствором меди с индикатором ПАН. Кристиансен [ 61 ( 44) ] сначала титрует Fe при рН 2 до перехода синей окраски 3-оксинафтойной кислоты в желтую, затем продолжает титрование при рН4 - 5 в ультрафиолетовых лучах до изменения флуоресценции от синей к зеленой. [13]
Особым вниманием в последнее время пользуются методы прямого титрования. Они проводят титрование в кипящем сильноуксуснокислом растворе с рН 3 и CuY - ПАН в качестве индикатора. Тихонов [ 62 ( 88) ] обнаружил некоторую тенденцию метода к заниженным результатам и предложил устанавливать раствор ЭДТА по стандартному раствору AI, если необходима большая точность определений. Ива-мото [ 61 ( 66) ] отмечает, что винная кислота при титровании не мешает и даже создает благоприятные условия, препятствуя заметному образованию гидроксосоединений. Титрование проводят в кипящем растворе при рН 3 7, причем в качестве индикатора вместо ПАН используют, благодаря лучшей растворимости, ПАР. Тейс [ 55 ( 26) ] и Пауль [ 56 ( 28) ] описывают прямое титрование с хромазуролом S в ацетатной буферной среде с. Тейс предпочитает проводить обратное титрование раствором соли алюминия. В аналогичных условиях, согласно Тэйлору [ 55 ( 8) ], проводят определение с применением гематоксилина в качестве индикатора. Автор избегает трудностей, связанных с нечеткой точкой эквивалентности, титруя известное количество комплек-сона анализируемым раствором. Неудобство этого метода очевидно. Кристиансен [ 61 ( 44) ] применяет флуоресцентную индикацию точки эквивалентности. В глициновом буферном растворе с рН 3 в ультрафиолетовых лучах А1 дает с 3-оксинафтойной кислотой синюю флуоресценцию, которая в точке эквивалентности переходит в зеленую. Необходимо подогревать раствор до 50 С, чтобы ускорить переход окраски. [14]
Страницы: 1