Летучесть
Cтраница 3
Летучесть / и активность а общепринято трактовать как эффективное давление и эффективную концентрацию. Это в общем правильно, если в данном случае под эффективностью понимать просто замену реальных величин давления р и концентрации с воображаемыми гипотетическими величинами / и а, причем такими, чтобы химический потенциал реальных веществ выражался через эти величины в точно такой же простой форме, в какой химический потенциал идеальных газов и идеальных растворов выражается через давление и концентрацию. [31]
Летучесть f представляет собой исправленное давление, после подстановки которого в уравнения идеальных газов или растворов они становятся пригодными для описания свойств реальных газов и растворов. [32]
Летучести каждого из компонентов в разных фазах при равновесии равны между собой. Если же, например, газовая фаза не насыщена жидкостью, то летучесть газа будет больше и растворимость газа в жидкости также будет больше, чем при равновесии. Наоборот, если при растворении хорошо растворимого газа не достигнуто насыщение жидкой фазы, то получается аналогичная ошибка в определении растворимости жидкости в сжатом газе. [33]
Летучесть, играющая существенную роль в процессах теплового инициирования взрыва, не может, однако, практически сказаться на чувствительности ВВ к удару и тем более на восприимчивости их к детонации под действием инициатора, поскольку разогревы и инициирование взрыва в этих случаях осуществляются в условиях очень высоких давлений, при которых испарение целиком или почти полностью подавляется. [34]
Летучесть / представляет собой исправленное давление, после подстановки величины которого формулы, описывающие свойства идеальных газов, становятся пригодными для описания свойств и поведения реальных газов. Таким образом, метод Льюиса представляет собой формальный прием, позволяющий использовать уравнения, описывающие свойства идеальных газов, для реальных систем. Но при этом возникает необходимость экспериментального определения значений / при различных давлениях и температурах для каждого реального газа. [35]
Летучесть может быть вычислена по этому уравнению. [36]
Летучесть - легкость, с которой продукт испаряется, летучие вещества имеют относительно высокую упругость паров и, таким образом, кипят при сравнительно низких температурах. [37]
Летучесть по этиловому эфиру ( или ксилолу) показывает скорость испарения испытуемого растворителя ( разбавителя) по сравнению со скоростью испарения этилового эфира, принятой за единицу. Чем выше этот показатель, тем медленнее испаряется растворитель и тем медленнее сохнет лакокрасочный материал, изготовленный на данном растворителе. [38]
Летучесть совпадает с давлением, если последнее настолько мало, что газ становится идеальным. [39]
Летучесть определяется давлением пара разделяемых компонентов; она полностью независима от выбора условий разделения, за исключением незначительного изменения с температурой, и поэтому не учитывается химиком-аналитиком. Иначе обстоит дело с селективностью: отношение коэффициентов активности отражает все возможные взаимодействия молекул разделяемых компонентов с неподвижной фазой; оценка этого отношения должна быть решающей для выбора характеристик, определяющих процесс разделения. Селективность неподвижной фазы часто задается в виде коэффициента селективности ОА / в Y B / V A гипотетических веществ А и В, которые имели бы одинаковое давление пара при рабочей температуре колонки и принадлежали бы к разным гомологическим рядам А и В. [40]
Летучесть является часто очень полезным свойством, позволяющим без труда удалить вещество, применявшееся для создания градиента, после окончания опыта. Сахароза, глицерин, этиленгликоль не летучи. Возможно, что подходящим окажется этиленбромгидрин ( р 1 77 г / см3, температура кипения 150 С), который уже применялся при ультрацентрифугировании. [41]
Летучесть с водяным паром часто зависит от строения вещества. Так, например, о-нитрофенол, в котором может образовываться внутримолекулярная водородная связь за счет взаимодействия заместителей, находящихся в о / 7 / по-положении, летуч с водяным паром. [42]
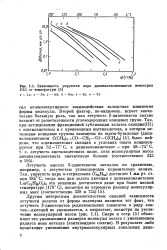 |
Зависимость упругости пара дипивалоилметанатов некоторых РЗЭ от температуры. [43] |
Летучесть многих ( 3-дикетонатов металлов по сравнению, например, с летучестью углеводородов поразительно велика. [44]
Летучесть уменьшается от йодистых до хлористых соединений, и в том же направлении возрастает устойчивость. [45]
Страницы: 1 2 3 4