Лецитиназ
Cтраница 1
Лецитиназы ( их две - А и В) отщепляют от лецитина высокомолекулярные жирные кислоты, предельную и непредельную, по месту их связи с глицерином. [1]
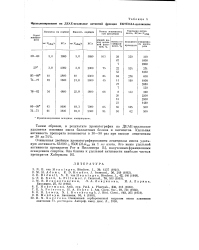 |
Фракционирование на ДЕАЕ-целлюлозе активной фракции ЕКТЕОЛА-целлюлозы. [2] |
Очищенная двойным хроматографированием лецитиназа имела удельную активность 63 000 9500 DLmwo на 1 мг азота. [3]
К первой подгруппе следует отнести липазы, лецитиназы, эстеразу холестерина, холинэстеразу и хлорофиллазу; ко второй-фосфатазы и сульфатазы. [4]
Установлено, что потенциальная инсектицидная активность шести видов бацилл ( Вас. АТСС 4633)) зависит не от наличия протеиназы и лецитиназы, а от присутствия сс-экзотоксина; для Вас. Hi-серотип) дополнительный эффект оказывает р-токсин. [5]
С), который разрушает фосфолипиды в тканях, тогда как В. Другой токсичный компонент был обнаружен Мак-Коннелом и Ричардсом [1334] в культурах В. Он отличается от лецитиназы и от нетермостойкого токсина тел включений большей стойкостью к нагреванию и токсичен при инъекции, но не при скармливании. [6]
В большинстве это ферменты, которые используются бактерией для получения питательных веществ и которые она выделяет в культуральную жидкость. С ( лецитиназу С) и убедительно доказал ее связь с инсектицидной активностью. [7]
С, ( фосфолнпаза С, а-токсин) - катализирует гидролитич. Лецитиназа ( 1 входит в состав бактериальных токсинов. Попы On, Si1, Fe н Ва сильно тормозят этот фермент. В небольших количествах Лецитиназа С обнаружена в связанном состоянии в тканях животных, в частности в тканях мозга. [8]
Лецитиназа С ( фосфолипаза С, а-токсин) - катализирует гидролитич. Лецитиназа С входит в состав бактериальных токсинов. Ионы Си, Sr, Fe И Ва сильно тормозят этот фермент. В небольших количествах лецитиназа С обнаружена в связанном состоянии в тканях животных, в частности в тканях мозга. [9]
Так, Clostridium welchii - палочкообразный микроб, обычно обнаруживаемый при газовой гангрене, - выделяет фермент, называемый лецитиназой. Он разрушает эритроциты, разлагая вещество лецитин, имеющееся в их оболочке. Яд кобры и гремучей змеи также содержит лецитиназу. Тот же микроб выделяет еще и фермент, который растворяет белок соединительной ткани мышц, а газ, выделяющийся при газовой гангрене, образуется в результате действия группы ферментов, ускоряющих патологическую разновидность брожения. Действие многих препаратов и ядов также связано с ферментативными реакциями. [10]
Последние обладают сильным гемолитич. Лецитиназа А содержится в соке поджелудочной железы животных и человека. Очень активная лецитиназа А содержится в ядах нек-рых насекомых и змей ( скорпионов, пчел, ос, кобр), с чем связано их токсич. А, сразу же инак-тивируются в результате действия на них лецитиназы В. [11]
Штамм entomocidis Heimpel et Angus [92] был выделен Штейнхаузом [180] из Aphomia gularis Zell. Помимо этого, сюда относится другой штамм, выделенный из Plodia interpunctella Hbn. Штейнхаузом [180] и описанный Хеймпелом и Ангусом в 1958 г. как В. Оба названных штамма характеризуются отрицательной реакцией Воже-Проскауера, не образуют лецитиназу и происходят из одной географической области. Первый штамм патогенен для тутового шелкопряда, второй можно применять против гусениц белянки. [12]
Страницы: 1