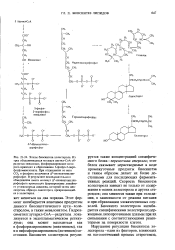
Мевалонат
Cтраница 1
Мевалонат можно получить восстановлением эфира 3-гид-рокси - 3-метил - 5 5-диметоксипентановой - 1 кислоты [ 3Н ] борогидри-дом лития с последующим окислительным гидролизом или восстановлением альдегидной группы мевалдиновой кислоты [ см. формулу ( 28) ] [ 3Н ] борогидридом натрия. [1]
С ] Мевалонат и эпоксисквален включаются в 3-амирин ( 68) и родственные тритерпены в проростках гороха. Радиоактивная метка из положения С-2 в мевалонате попадает в экваториальную метильную группу при С-4. Шесть три-тиевых меток включаются в р-амирин из [ 4 () - 4 - 3H 2 - MCJ мевало-новой кислоты, и их положение, особенно в кольце Е, определяется последовательностью 1 2-водородных сдвигов в соответствии с этой схемой. [2]
Применение таких мевалонатов обеспечивает включение метки в определенные места конечных терпеноидов. [3]
Синтез сквалена из мевалоната. Метаболический путь превращения ме-валоната начинается с его активации под действием трех АТФ-зависимых ки-наз. Вначале мевалоновая кислота фосфорилируется АТФ по гидроксигруппе в положении 5, в результате чего образуется 5-фосфомевалонат, который затем при затрате еще одной молекулы АТФ превращается в 5-пирофосфомевалонат. [4]
Необратимая реакция образования мевалоната определяет скорость синтеза холестерина. Активность ГМГ-редуктазы и скорость синтеза холестерина ускоряются при снижении содержания холестерина в печени, пище, при Действии радиации, введении тироидных гормонов, инсулина. Угнетение активности ГМГ-редуктазы отмечается при голодании, тироидэктомии, введении холестерина, глюка-гона, глюкокортикоидов. [5]
Кроме того, включение мевалоната в два пятиуглеродных фрагмента Сю-скелета часто не равноценно. В случае камфоры ( 84) большая часть радиоактивной метки из [ 2 - иС ] мевалоновой кислоты находится в положении 6, в то время как у пулегона ( 85) метка распределяется между двумя положениями. Как и в случае туйона, содержание метки в той части соединений, которые образовались из диметилаллилпиро-фосфатз, весьма невелико. [6]
Последняя реакция является ключевой стадией в биосинтезе мевалоната. [7]
Вызывает блокирование синтеза холестерина in vivo из мевалоната с накоплением десмостеро-ла. [8]
При изучении биосинтеза с использованием стереоспецифически меченных тритием мевалонатов показано, что гидроксилирование кольца А происходит с сохранением конфигурации при С-3 и что образование двойной связи в кольце А происходит в результате цмс-элиминирования атома водорода с а-стороны молекулы. Изучен метаболизм ряда гиббереллинов, например А, и А2, в высших растениях. [9]
Мевалдиновая кислота ( 28), хотя и восстанавливается в мевалонат специфической редуктазой, вероятно, не является нормальным интермедиатом в биосинтезе мевалоната. Обе стадии восстановления, приводящие к превращению ( 24) в мевалоновую кислоту ( 3) и катализируемые ГМГ-КоА-редуктазой, связаны с участием 4-рго - ( R) - водородного атома NADP. Представляет интерес стереохимия этого восстановления. Полутиоацеталь ( 27) как аддукт З () - мевалдиновой кислоты и кофермента А служит хорошим субстратом для ГМГ-КоА-редуктазы печени крысы, и его восстановление приводит к 5 - pro - ( S) - меченному соединению. В то же время, восстановление 3 ( R) - мевалдиновой кислоты мевалдинатредуктазой из печени крысы приводит к b - pro - ( R) - меченному соединению. [10]
Некоторые из этих методов пригодны для синтеза нестереоспеци-фично меченных тритием мевалонатов. Так, из метил [ 2 - 3Н2 ] бром-ацетата методом Реформатского получают [ 2 - 3H2J мевалонат. [11]
Этот фермент ингибируется конечным продуктом данного биосинтетического пути-холе-стеролом, а также мевалонатом. Гидрок-симетилглутарил - СоА - редуктаза локализуется в эндоплазматическом ретику-луме; она может находиться как в фосфорилированном ( неактивном), так и в нефосфорилированном ( активном) состоянии. [13]
При озонолизе сквалена, полученного биосинтетически из [ 5 - 2Н2 ] мевалоната, образуется тридейтероянтарная кислота с ( S) - конфигурацией. Это позволило предсказать, что тритий, включенный в сквален из [ 3Н ] NADP может в конце концов появиться в С-11 сс - и С-12 ( 3-по-ложениях стероидных ядер. При использовании 1 ( R) - [ 1 5 9 - 2Н3 ] фар-незилпирофосфата, полученного из [ 5 ( /) - 5 - 2Н ] мевалоната, было показано, что не происходит потери этой метки при биосинтезе сквалена и что каждый из центральных углеродных атомов сохраняет свою метку. Таким образом, при образовании сквалена теряется 1 - pro - ( S) - водородный атом фарнезилпирофосфата. Кроме того, дидейтероянтарная кислота, полученная озонолизом сквалена, была оптически неактивным мезо - ( % 5) - изомером. Таким образом, соединение двух молекул фарнезилпирофосфата ( 34) приводит к сквалену ( 6) с сохранением конфигурации при С-1 в одной молекуле и с обращением конфигурации при С-1 в другой. [14]
Этот водородный атом, как и следовало ожидать, берется из С-4-положения мевалоната; действительно, 4 - pro - ( S) - водородный атом мевалоната локализован у атома С-8. Кроме того, оба атома водорода при С-1, атом водорода при С-5 и оба атома водорода при С-6 метятся соответствующими мева-лонатами. Эти результаты подтверждают постулированный гид-ридный сдвиг и исключают участие А1 10 -, Д510 - и А5 6-интермедиа-тов в биосинтезе. Следовательно, С-10-карбениевый ион может быть стабилизирован взаимодействием с нуклеофилом до лакто-низации. [15]
Страницы: 1 2 3 4