Надокись
Cтраница 1
Надокись и озонид натрия получены совсем недавно и существуют лишь в замороженном состоянии. [1]
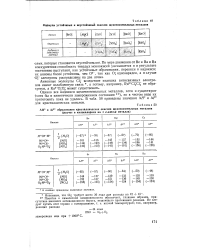 |
Формулы устойчивых и неустойчивый окислов щелочноземельных металлов. [2] |
Однако все надокиси щелочноземельных металлов, хотя и существуют хотя бы в кинетически замороженном состоянии), но в чистом виде их приготовить пока не удалось. В табл. 50 приведены значения АЯ и AF для кристаллических окислов. [3]
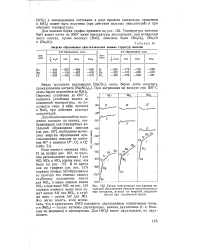 |
Схема, поясняющая ход кривых энтальпий образования окислов щелочноземельных металлов, исходя из энергий, выделяющихся при соединении ионов. [4] |
Перекись устойчива до 600 С, надокись устойчива вплоть до комнатной температуры, но получается лишь в виде примеси к ВаО2 при действии сильных окислителей. [5]
Такие формулы он приводит для соединений надокиси и закиси урана, его зеленой окиси, которая в случае U 120 была бы аналогом FeO Рв20з, а в случае U 240 - аналогом Мо02 - 2МоОз, и, наконец, соединений окиси урана. [6]
Окись лития [ Li2O ] устойчива; перекись лития [ Li2O2 ] разлагается с выделением части своего кислорода уже при 160; надокись [ LiO2 ] очень неустойчива, и первые сведения о ней получены совсем недавно. [7]
После изучения некоторых характеристик одноатомных анионов, образуемых кислородом, рассмотрим двухатомные анионы Ог и О2, необходимые для понимания кристаллических перекисей и надокисей металлов, например [ Na2O2l или [ КО21, в структурах которых анионы О2 и Of стабилизуются. [8]
По мере движения от Be к Ва и Ra конкурентная способность твердых моноокисей уменьшается и в результате постепенно выступают, как устойчивые образования, перекиси и надокиси; их анионы более устойчивы, чем О2 -, так как О-2 однозаряден, а в случае О - электроны распределены на два атома. [9]
Браунер считает, что они, может быть вообще недостижимы, однако ученый полагает, что их можно получить, если в качестве кислородоносителей присутствуют другие высшие окислы этой группы. Браунер не считает такие окислы настоящими надокисями или перекисями; они ( за исключением церия) не образуют солей. Скорее всего они имеют характер озонидов. Тем не менее в рассуждениях Браунера заключается одна мысль, которую ученый прямо не высказывает, но ее можно прочитать между строк. Редкоземельные элементы представляют крайне своеобразную область периодической системы. До сих пор ученые имели здесь дело, как правило, с окислами, зная свойства лишь некоторых металлов и то весьма слабо, и строили свои рассуждения только исходя из свойств окислов. В данном случае этого недостаточно, чтобы решить вопрос о принадлежности элемента к той или иной группе. [10]
Другим путем, дающим возможность составления известного представления о строении пернитрида бария, является определение его-магнитной восприимчивости. Можно полагать по аналогии с перекисями и надокисями, что пернитрид бария образует ионную решетку. Рассмотрим с этой точки зрения некоторые возможные модели. [11]
Окислы щелочноземельных металлов представляют собой труднолетучие соединения и лишь некоторые из них переходят в газообразное состояние без разложения. Так, например, твердые перекиси [ МО2 ] и еще более неустойчивые надокиси [ МО4 ] разлагаются раньше, чем начнется испарение. Недокиси ( М2О), наоборот, в твердом состоянии неустойчивы, но зато открыты при высоких температурах в виде газообразных молекул. [12]
На рис. 156 приведены ДЯ образования из простых тел. Энергия связей и, следовательно, крутизна хода, например, линии твердых окислов магния оказалась недостаточной для того, чтобы покрыть эндоэффект ато-мизации простых тел. В результате надокись [ MgOj - вещество неустойчивое, распадающееся с образованием [ MgO2l экзотермически. [13]
 |
Относительная активность окислов в разложении закиси азота, представленная в виде температуры, при которой реакция впервые становится заметной. [14] |
Иными словами, электроны, возникающие на стадии десорбции, в данном случае легко поглощаются положительными дырками валентной зоны. Обращаясь к более новым исследованиям индивидуальных окислов, можно найти возражения против предположения, что определяющей скорость стадией является десорбция. То, что активность окислов-изоляторов MgO и СаО оказалась промежуточной между активностью р - и - полупроводников, представляется довольно неожиданным, хотя некоторые соображения по этому поводу можно высказать на основании того факта, что редкоземельные окислы дают устойчивые ионные надокиси. [15]
Страницы: 1 2