Наклон - кривая - титрование
Cтраница 2
Поскольку и относительная точность, и буферная емкость находятся в обратной зависимости от наклона кривой титрования в конечной точке, обе эти величины тесно связаны между собой. [16]
Обычный способ определения конечной точки в потенциометрическом титровании основывается на том факте, что для нее наклон кривой титрования максимален. Это дает очень хорошее приближение к точке эквивалентности даже в разбавленных растворах или когда разность потенциалов между парами окислителя и восстановителя мала. [17]
Согласно Фритцу [ 59 ( 96), можно весьма селективно оттитровать Sc, если вместо визуальной индикации с комплексообразую-щим индикатором применить фотометрическую индикацию точки эквивалентности с медью в качестве индикатора по наклону кривой титрования ( см. стр. Титрование проводят при рН2 7 и длине волны 745 нм. [18]
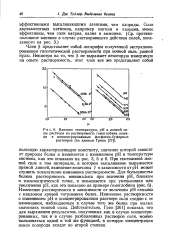 |
Влияние температуры, рН и ионной силы раствора на растворимость гемоглобина лошади в концентрированных фосфатно-буферных растворах ( по данным Грина. [19] |
При постоянной ионной силе ъ том интервале, в котором высаливание выражается прямой линией, изменение величины Р в зависимости от рН может служить показателем изменения растворимости. Изменение растворимости в зависимости от величины рН связано с наклоном кривой титрования белка. Изменение растворимости с вменением рН в концентрированном растворе соли сходно с ее изменением, наблюдаемым в случае того же белка при малых значениях ионной силы. Действительно, Грин [201] показал, что для выражения результатов, полученных как в случае концентрированных, так и в случае разбавленных растворов соли, можно пользоваться одной и той же функцией, в которую концентрация ионов водорода входит во второй степени. [20]
Точка, при которой начинается регулирование, может быть заранее установлена оператором. В некоторых приборах скорость поступления реагента регулируется по тангенсу угла наклона кривой титрования. [21]
Образуется самоиндицирующая система магний - калмагит, являющаяся индикатором по наклону кривой титрования для Са2 - иона, который практически не реагирует с красителем. Поскольку кальций сильнее связывается с ЭДТА, чем магний, он титруется сначала, и получают кривую титрования, состоящую из трех частей: горизонтальной, наклонной и снова горизонтальной. Первый перегиб кривой соответствует окончанию титрования кальция, второй - окончанию титрования магния. [22]
Например, при титровании ионов ванадила раствором сульфата церия ( IV) кривая титрования имеет вид, изображенный на рис. 7: вначале повышение силы тока обусловлено восстановлением ванадия ( V), образующегося во время титрования ( за счет окисления ванадила церием), а затем, после точки эквивалентности, - восстановлением избыточного церия. Так как коэффициенты диффузии ионов VO3 и Се4 различны, то различен и наклон кривой титрования до и после конечной точки. [23]
Например, при титровании ионов ванадила раствором сульфата церия ( IV) кривая титрования имеет вид, изображенный на рис. 7: вначале повышение силы тока обусловлено восстановлением ванадия ( V), образующегося во время титрования ( за счет окисления ванадила церием), а затем, после точки эквивалентности, - восстановлением избыточного церия. Так как коэффициенты диффузии ионов V03 и Се4 различны, то различен и наклон кривой титрования до и после конечной точки. [24]
Значительно более удобно, согласно Флашке [ 62 ( 26) ], титрование раствором ГЭДТА, так как в этом случае уже с самого начала константы комплексов с цинком и кадмием отличаются друг от друга почти на два порядка. И здесь Си2 - ионы в сильно аммиачном растворе используются в качестве индикатора, связываясь в комплекс после ионов кадмия до или совместно с ионами цинка, вызывая изменение наклона кривой титрования. [25]
В непосредственной близости к значению Ф1 начинает выпадать в осадок AgCN и эти уравнения больше не применимы. В этой точке происходит резкое изменение наклона кривой титрования. [26]
 |
Графический метод определения точки эквивалентности по кривым титрования. [27] |
Определение точки эквивалентности по изгибу кривой также не лишено недостатков. В ряде случаев получаются очень крутые кривые с весьма неясно выраженным перегибом, что затрудняет определение. Точку эквивалентности можно установить наиболее точно по изменению наклона кривой титрования. Точка пересечения перпендикуляра, опуш енного из точки максимума, с абсциссой дает точку эквивалентности Т в единицах напряжения. [28]
Краситель прибавляют в избытке по отношению к цинку. Комплекс цинка с красителем является индикатором на кадмий по наклону кривой титрования. По двум перегибам на кривой титрования можно вычислить соответствующий - расход комплексона на титрование кадмия и цинка. [29]
Исключение влияния теплоты разбавления титранта, произведенное с помощью дифференциального метода, может быть неполным, так как в сравнительном растворе титрант не вступает в реакцию с определяемым веществом. Электрическая калибровка прибора позволяет вести простой расчет теплоты реакции. В связи с тем что сигнал, поступающий в цепь от титруемого раствора, линейно зависит от изменения температуры раствора, лучше измерять не общую выделяющуюся теплоту реакции, а только наклон кривой титрования. [30]
Страницы: 1 2 3