Наличие - специфическая адсорбция
Cтраница 2
В случае обратимых электродов разность химических потенциалов участвующих в электродной реакции ионов на электроде и в растворе не зависит от наличия специфической адсорбции ионов, в связи с чем равновесный потенциал электрода такой же, как при отсутствии специфической адсорбции. [17]
В случае обратимых электродов разность химических потенциалов, участвующих в электродной реакции ионов на электроде и в растворе, не зависит от наличия специфической адсорбции ионов, в связи с чем потенциал электрода такой же, как в отсутствие специфической адсорбции. [19]
Величина ра, входящая в уравнение (8.4), зависит от концентрации раствора и температуры, величина pi - от концентрации раствора, температуры, наличия специфической адсорбции и других факторов. [20]
Величина ра, входящая в уравнение (8.4), зависит от концентрации раствора и температуры, величина ifi - от концентрации раствора, температуры, наличия специфической адсорбции и других факторов. Величины ( ра и г н зависят также от силы постоянного тока, проходящего через границу раздела электрод - раствор. [21]
Выполнение этих условий может быть связано с малостью величины sac, а также с наличием разных знаков у величин 5аои sap, что возможно при наличии специфической адсорбции у поверхности разрыва. [22]
Если предположить, что адсорбция происходит только за счет электростатического взаимодействия катионов ингибитора с отрицательно заряженной поверхностью металла через слой молекулярного сероводорода, то поскольку слой сероводорода может только ослабить это взаимодействие, эффективность защиты в этом случае должна была бы несколько снизиться, Следует допустить поэтому наличие специфической адсорбции катионов ингибитора на поверхностном слое сероводорода. Адсорбируясь на слое сероводорода, катионоактивный ингибитор создает энергетический барьер за счет ф - - потенциала, который препятствует подводу ионов гидроксония. Ингибитор таким образом блокирует молекулы сероводорода, уменьшая образование ионов сульфония. [23]
А не зависит от заряда электрода. При наличии специфической адсорбции заряд электрода и специфически адсорбированный заряд входят в выражение для j2 - В разбавленных растворах j2 может настолько отличаться от фт, что а0 будет отличаться от а5 на целый порядок. В таком случае при определении R изменения величины fa можно сравнить по важности с основным членом фт - Это особенно проявляется при электровосстановлении анионов [4, 11], когда ток вначале возрастает ( с ростом отрицательного потенциала), затем падает вблизи потенциала нулевого заряда и вновь возрастает. [24]
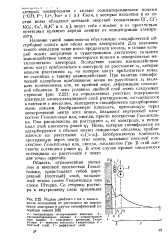 |
Модель двойного счоя и зависимость потенциала от расстояния до поверхности электрода в случае специфической адсорбции аниона. [25] |
Наличие такой зависимости обусловлено специфической адсорбцией одного или обоих ионов электролита Для описания такого поведения чаще всего предлагали модель, в основе которой лежит допущение о существовании достаточно сильного взаимодействия между некоторыми ионами и поверхностью металлического электрода Вследствие такого взаимодействия ионы могут приблизиться к электроду на расстояние jq, которое меньше расстояния jcj, на которое Moiyr приблизиться ионы, не склонные к такому взаимодействию. При наличии специфической адсорбции приближение ионов на расстояние х вызывает исчезновение или, по крайней мере, деформацию сольват-ной оболочки. В этих условиях двойной слой имеет следующее строение ( рнс 2.22): на определенных участках поверхности электрода мономолекулярный слои растворителя, находящеюся в контакте с металлом, замещается специфически адсорбированными ионами. Воображаемую плоскость, проходящую через электрический центр этих ионов, называют внутренней плоскостью Гельмгольца или, иногда, просто плоскостью Гельмгольца. Воображаемую плоскость, проходящую через центр этих ионов, называют внешней плоскостью Гельмгольца или, иногда, плоскостью Гци В этой плоскости потенциал равен ф2 В этом случае кривая зависимости потенциала от расстояния х имеет две точки перегиба. [26]
Еще Смолуховский в 1903 г. обратил внимание на то, что в диафрагме, капилляре или в коллоидной системе раствор электролита должен вести себя так, как будто его электропроводность больше, чем получается при обычных измерениях в том же электролите в отсутствие двухфазной границы. Как известно в настоящее время, физическая причина повышенной электропроводности в капилляре заключается, во-первых, в том, что при наличии специфической адсорбции электролита на поверхности при образовании двойного слоя общее количество ионов, переносящих электричество в капилляре, отличается от количества ионов в равном объеме той же жидкости вне капилляра, и, во-вторых, в том, что при прохождении тока через диафрагму сам раствор движется, причем вместе с жидкостью перемещаются заряды подвижной части двойного слоя, что равнозначно дополнительному прохождению электрического тока. [27]
Величины W могут быть, вообще говоря, как положительными, так и отрицательными. Для электродных реакций, если реагенты не обладают специфической адсорбируемостью, W zety, где z - заряд соответствующего иона. При наличии специфической адсорбции W включает также неэлектростатический член. [28]
При наличии специфической адсорбции анионов в этих растворах изменение потенциала происходит иначе; оно показано на рис. 12 сплошной кривой. В растворе KJ поверхность заряжена положительно, к пей в избытке притянуты анионы, и образующийся слой правильнее было бы назвать тройным электрическим слоем. [29]
В работе [14] Парсонс предположил, что эффект Есина - Маркова можно объяснить, исходя из изотермы Темкина. Однако в рамках вывода этой изотермы остаются не ясными вопросы, связанные с корректным учетом дальнодействующих кулоновских сил. В отличие от этого, выведенная здесь изотерма адсорбции для ионов правильно учитывает силы электростатического взаимодействия между ионами и металлической фазой и позволяет объяснить экспериментально наблюдаемые закономерности на границе ртуть / раствор при наличии специфической адсорбции ионов. [30]
Страницы: 1 2 3

