Анализ - поляризационная кривая
Cтраница 2
Методы поляризационной коррозиометрии, основанные на анализе поляризационных кривых, получаемых при поляризации электрода внешним током, общеизвестны. Однако этот метод имеет ограничения, связанные с необратимыми изменениями электродной системы в процессе измерений при значительной поляризации. Развитием этих методов явилась разработка смежных методов, позволяющих существенно уменьшить поляризацию электрода и определить все три параметра коррозионного уравнения ( Ь3 и Ьк, гкор) в одном эксперименте. [16]
Оптимальное значение потенциала электрода выбирается на основании анализа соответствующих поляризационных кривых, имеющихся в работах по полярографии или специально снятых перед проведением электролиза. [17]
Установление природы поляризации при разряде катионов одного сорта производится анализом экспериментальных поляризационных кривых. Один из таких методов анализа сводится к установлению подчинения экспериментальных данных уравнениям зависимости ( 8) - ( 11) между скоростью процесса и потенциалом электрода или перенапряжением выделения металла на катоде. [18]
В стационарных методах исследования параметры электрохимических реакций определяют на основе анализа поляризационных кривых, не изменяющих свою форму во времени. Если на электрод задают определенное значение потенциала и фиксируют установившееся во времени значение плотности тока, то такой метод называется потенциостатическим. [19]
Кинетический анализ зависимости фототока от потенциала электрода, концентрации акцептора, рН раствора, а в некоторых случаях также и от времени аналогичен анализу обычных поляризационных кривых. [20]
Результаты длительных коррозионных испытаний рассмотренных материалов в средах пилотной установки, имитирующей работу реактора, и колонной аппаратуры ( окисления хлористого нитрозила и хлор-ионов, а также осушки смеси газов) полностью соответствуют выводам, полученным из анализа поляризационных кривых. Титан и его сплавы, за исключением сплава 4200, имеющего высокую скорость общего растворения, и сплава 4202, подверженного питтинговой коррозии, стойки во всех жидких и газообразных средах. Стали и никель подвержены значительной общей и локальной коррозии. Никелевые сплавы показали низкую скорость разрушения при заметной локальной коррозии, в то время как кремнистый чугун не подвержен в этих условиях локальной коррозии, а скорость его общего разрушения в 5 - 10 раз ниже соответствующей величины для никелевых сплавов. [21]
 |
Макростуктуры сварных контактно-роликовых швов ( х 50. [22] |
Для сварных соединений, полученных контактно-роликовой сваркой, были проведены электрохимические поляризационные исследования. Из результатов анализа поляризационных кривых, сведенных в табл. 4, следует, что сварные соединения, полученные с частотой сварочного тока 25 имп. [23]
Далее строят парциальные поляризационные кривые, а также суммарную поляризационную кривую и сравнивают ее с экспериментально полученной. На основании анализа поляризационных кривых делают заключение о механизме электродного процесса. [24]
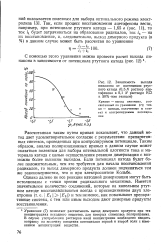 |
Зависимость выхода пинакона от потенциала ртутного катода ( 0 5 N раствор ацетофенона в 0 1 Л растворе КС1 в 50 % - ном этаноле. [25] |
Рассчитанная таким путем кривая показывает, что данный метод дает удовлетворительное согласие с результатами препаративных синтезов, проведенных при контролируемом потенциале. Таким образом, анализ поляризационных кривых в данном случае может оказаться полезным для выбора оптимальной плотности тока и материала катода с целью осуществления реакции димеризации с возможно более высоким выходом. Если потенциал катода будет более положительным, чем это требуется для начала восстановления радикалов, то выход димерного продукта должен подчиняться тем же закономерностям, что и при электросинтезе Кольбе. [26]
Исследования проводят методом получения и анализа потенциодинамиче-ских поляризационных кривых. Применяют потенциостаты П-5848 или П-5827 М с автоматической записью кривых на потенциометре КСП-4 или ПДф-002. Используют электрохимическую ячейку без разделения анодного и катодного пространства. [27]
Полученные в данной работе кинетические данные показывают сложный характер влияния экспериментальных условий на процесс электровосстановления нитрогруппы. Следуем отметить, что наблюдается аналогия в характере влияния плотности тока, температуры, концентрации кислоты и деполяризатора на интенсивность восстановительного процесса и на выхода метаниловой кислоты для платинового и медного катода. Из анализа поляризационных кривых следовало ожидать, что образованию метаниловой кислоты благоприятствуют низкие плотности и определенный диапазон концентраций серной кислоты. Кинетические данные, полученные двумя методами, находятся в определенном соответствии. [28]
В этой области перенапряжений зависимость между / о и 1 линейна и не зависит от коэффициента переноса. Достаточно надежная оценка плотности тока обмена по этому уравнению возможна, если последняя, по крайней мере, на порядок ниже предельной диффузионной плотности тока. Далее для анализа поляризационных кривых необходимо установить природу предельной плотности тока. На вращающемся дисковом электроде значение предельной диффузионной плотности тока прямо пропорционально корню квадратному из частоты вращения диска. Для кинетических предельных токов ( определяемых замедленностью стадии гомогенной или гетерогенной химической реакции) значение предельной плотности тока не зависит от перемешивания. Поправка в уравнениях электрохимической кинетики на предельную плотность тока не зависит от его природы, так как возникновение перенапряжения диффузии и химической реакции связано с изменением концентрации. [29]
Процессы анодного окисления органических веществ изучены в значительно меньшей степени, чем катодные процессы. Анализ механизма этих процессов почти всегда затрудняется тем, что анодное окисление органических соединений часто сопровождается растворением материала анода или образованием на его поверхности окисных слоев. Это приводит к изменению состояния анодной поверхности в ходе электролиза и существенно ограничивает возможности анализа поляризационных кривых. [30]
Страницы: 1 2 3