Пентафторид - хлор
Cтраница 1
Пентафторид хлора обладает высокой упругостью паров и значительно меньшей реакционной способностью, чем трифторид хлора. С водой не реагирует так бурно, как трифторид хлора. [1]
Пентафторид хлора сильно токсичен, и все меры предосторожности, относящиеся к трифториду хлора, надо относить и к нему. Коррозионная активность окислителя, по-видимому, будет меньше чем у трифторида хлора, но конструкционные материалы должны использоваться те же. [2]
Пентафторид хлора пока еще очень мало изучен как окислитель для ракетных топлив, и поэтому применение его должно производиться с большой осторожностью. [3]
Пентафторид хлора ( пд - 100 С) получен недавно при действии фтора на три-фторид хлора при 350 С и давлении 250 атм. [4]
 |
Инфракрасный спектр газообразного GIFs. [5] |
ИК-спектр пентафторида хлора ( рис. 31) был получен при использовании призмы из - Nad. Сходство ИК-спектров пентафторида хлора, пентафторида брома и XeOF4 указывает на то, что пентафторид хлора образует квадратную пирамидальную конфигурацию с атомом хлора, лежащим почти в плоскости четырех атомов фтора основания пирамиды. [6]
 |
Схема лабораторной установки для получения пентафторида хлора ( пат. США 3454476. [7] |
Выход пентафторида хлора значительно увеличивается, если вместо хлора в качестве исходного продукта используется трифторид хлора, вводимый в безводную плавиковую кислоту, содержащую незначительные количества фторида натрия или калия. Схема лабораторной установки для получения пентафторида хлора представлена на рис. 11.34. Электролизер 3 изготовлен из нержавеющей стали и имеет двойные стенки, между которыми ципкулирует хладоагент. [8]
Температура кипения пентафторида хлора равна - 129 С; теплота парообразования 5 74 ккал, константа Трутона 22 0 кал / К. [9]
Теплота образования пентафторида хлора определялась неоднократно. [10]
В связи с открытием пентафторида хлора рассматривается возможность его использования как окислителя ракетных топлив. [11]
Вспомните, что существуют моно -, три - и пентафторид хлора и что вряд ли способен к существованию в обычных условиях гептафторид хлора. Не могут семь атомов фтора разместиться вокруг небольшого по размерам атома хлора, образовав устойчивую молекулу. Почему мы говорим об этих соединениях. Они богаты фтором ( 79 и 87 %), что и привлекает к ним интерес как к весьма эффективным фторокислителям. Но, увы, теория полагает, что наш интерес чисто платонический: такие молекулы, как C1F7 и NF5, не будут устойчивыми. Если они и могут существовать, то только в экстремальных условиях, т.е. при очень низких температурах, что вряд ли устраивает практиков, производящих ракетное топливо. [12]
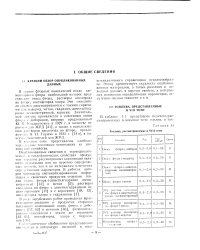
В таблице 2.7 приведены нормальные температуры кипения фтора, кислорода, окиси фтора, пентафторида хлора, диборана, модификаций водорода, метана, этана, хлора, грифчорида хлора, двуокиси хлора, азота и фтористого водорода, а также их теплоты испарения при этих температурах. Для двуокиси углерода приведены температура и теплота сублимации. [13]
 |
Топлива, рассматриваемые в VIII томе. [14] |
В группе фторных окислителей после элемент рного фтора наибольший интерес представляют окись фтора, растворы кислорода во фторе, пентафторид хлора. Эти окислители обычно рассматриваются с такими горючими как подо род, метан, гидразин, диметилгид-разин несимметричный, керосин. [15]
Страницы: 1 2 3