Пентахлорэтан
Cтраница 2
Аналогичным образом распадается и пентахлорэтан на катализаторах с другими носителями ( целит, силикагель) в условиях температур около 400 С. [16]
Сюда относятся тетрахлорэтан, пентахлорэтан. [17]
Полимеризация трифторхлорэтилена в растворе пентахлорэтана под действием - у-излуче-ния протекает быстрее, чем в блоке. Повышение температуры при полимеризации в растворе ведет к повышению скорости полимеризации. [18]
Установлена возможность полной регенерации отработанного пентахлорэтана щелочным раствором и полное извлечение 2 4 - Д кислоты из растворителя. [19]
Показана возможность повторного многократного использования пентахлорэтана как растворителя при хлорировании без предварительного освобождения от оставшейся в растворе 2 4 - Д кислоты и дихлорфенола. [20]
О получении ДДТ взаимодействием хлорбензола с пентахлорэтаном имеются лишь патентные указания29, но нет подробных данных об условиях проведения процесса и о всех побочных продуктах. [21]
По указанию патента конденсацию хлораля с пентахлорэтаном проводят при низкой температуре в присутствии катализаторов. В качестве катализаторов рекомендованы безводный хлористый алюминий, хлорное железо и хлористый цинк. [22]
Показано, что при хлорировании в пентахлорэтане содержание монохлоризомера в конечном продукте может быть сведено к 1 - 3 / о - значительно ниже чем при хлорировании феноксиуксусной кислоты в водной суспензии и расплаве, что практически не влияет на активность гербицидного препарата. [23]
Данные по кинетике газофазного каталитического процесса дегидрохлорирования пентахлорэтана и несимметричных хлорэтанов практически отсутствуют. Приведенный выше ряд свидетельствует, что они дегидрохлорируются, как правило, с большей скоростью, чем симметричные хлорэтаны. Можно отметить, что скорость дегидрохлорирования 1 1 - С2Н4С12 на оксиде алюминия при 340 С примерно в 1 5 раза выше, чем для 1 2 - С2Н4С12, а хлорид бария активирует процесс разложения пентахлорэтана на угле при 200 - 350 С. [24]
Тетрахлорэтилен ( перхлорэтилен) получают каталитическим дегидрохлорированием пентахлорэтана. [25]
Дифтор-2 - хлорэтилен получался действием фтористого водорода на пентахлорэтан согласно американт скому патенту 1970562 с последующим отщеплением двух атомов хлора с помощью цинка. [26]
Нилсен, Лианг и Дааш [1071] изучали спектр пентахлорэтана, произвели отнесение колебаний и рассчитали термодинамические функции при определенных температурах. Кобе и Харрисон [ 7761 опубликовали более полные расчеты на основании тех же отнесений. Смит, Бьеллерап, Крук и Уестермарк [1384] получили данные по энергии сгорания, которые после исправления с учетом нового значения энтальпии окисления мышьяковистого ангидрида [142] и приведения к Д - Нс298 дали ЛД / 298 ( 0 - - 45 3 ккал / молъ. Россини, Вагман, Эванс, Левин и Джаффе [1249] приводят значения Тт - 244 2 К, &. [27]
Такое строение подтвердил позднее Уэлли668, изучивший фторирование пентахлорэтана теоретическим количеством HF, необходимым для введения двух атомов фтора; процесс велся при ПО-120 С в присутствии галогенидов сурьмы в качестве катализатора. [28]
Нилсен, Лианг и Дааш [1071] изучали спектр пентахлорэтана, произвели отнесение колебаний и рассчитали термодинамические функции при определенных температурах. Кобе и Харрисон [776] опубликовали более полные расчеты на основании тех же отнесений, Смит, Бьеллерап, Крук и Уестермарк [1384] получили данные по энергии сгорания, которые после исправления с учетом нового значения энтальпии окисления мышьяковистого ангидрида [142] и приведения к АНс2о8 дали ДД / 298 ( 0 - 45 3 ккал / молъ. Россини, Вагман, Эванс, Левин и Джаффе [1249] приводят значения Тт 244 2 К, АНт 2 7 ккал / молъ, ТЪ 432 5 К и AHv 9 7 ккал / моль при температуре кипения. Если принять оценку & Ср испарения равной - 12 кал / ( моль - К), то AHv 2sfl 11 3 ккал / молъ и & Н / 9е ( g) - 34 0 ккал / моль, Киркбрайд [754] измерял энтальпию присоединения хлора к трихлорэтилену. Его данные в пределах ошибки эксперимента соответствуют результатам, полученным при изучении энтальпии сгорания. Курбатов [814] опубликовал данные по теплоемкости жидкости, которые, очевидно, слишком завышены. [29]
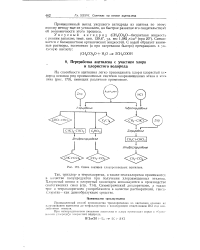 |
Схема синтезов хлорпроизводных ацетилена. [30] |
Страницы: 1 2 3 4