Замещение - поверхностная гидроксильная группа
Cтраница 1
Замещение поверхностных гидроксильных групп и атомов кислорода на атомы фтора и образование связей F - А1 - F усиливает электроно-акцепторные свойства поверхностных атомов алюминия. [1]
 |
Спектр ЭПР радикала -. SiOC ( CH3 2 [ на поверхности.| Спектр ЭПР радикала - т8ЮС ( СН3 аСНв ] на поверхности силикагеля при 77 К. [2] |
Эффективность замещения поверхностных гидроксильных групп силикагеля эфирными группами растет с повышением температуры. Полное этерифицирование поверхности удается провести при 100 - 500 С. [3]
Эффективность замещения поверхностных гидроксильных групп силикагеля эфирными группами растет с повышением температуры. [5]
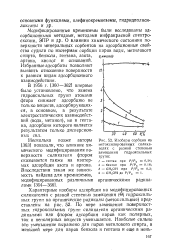 |
Изобары сорбции на метоксилированных силикагелях с разной степенью. [6] |
По мере замещения поверхностных гидроксильных групп силикагеля органическими радикалами или фтором адсорбция паров как полярных, так и неполярных веществ уменьшается. [7]
Сравнение спектров отравленного щелочными катионами и неотравленного образцов показало, что обработка катализатора не приводит к замещению поверхностных гидроксильных групп. [8]
Поэтому сопоставление активности и содержания хлора оказалось возможным только для образцов, прокаленных при 600, каталитическое - действие которых пропорционально содержанию в них хлора, i При активации соляной кислотой прежде всего наблюдает - ] ся частичное растворение окиси алюминия с образованием хло-I ристого алюминия, а также замещение поверхностных гидроксильных групп хлором. После декантации раствора в катализаторе остается некоторое количество хлористого алюминия. [9]
Еще в 1956 г. впервые было установлено [2], что замена поверхностных гидроксильных групп силикагеля атомами фтора снижает адсорбцию как полярных, так и неполярных молекул. По мере замещения поверхностных гидроксильных групп кремнезема органическими радикалами или фтором адсорбция паров как полярных, так и неполярных веществ уменьшается. Предельные сорбционные объемы пор адсорбентов при этом мало изменяются, за исключением определенных по воде. [11]
Однако в последние годы накоплен большой экспериментальный материал [1-13], указывающий на то, что изменение химической природы поверхности адсорбента путем проведения химических реакций приводит к изменению адсорбционной активности не только веществ, адсорбция которых является результатом электростатического взаимодействия, но и веществ, адсорбирующихся только в результате дисперсионного взаимодействия. Так, по мере замещения поверхностных гидроксильных групп си-ликагеля органическими радикалами или атомами фтора адсорбция паров как полярных, так и неполярных веществ уменьшается. Наиболее сильно это уменьшение выражено для паров воды, спиртов, в меньшей мере - для паров бензола и еще в меньшей степени для азота и аргона. [12]
Однако в последние годы накоплен большой экспериментальный материал [1-13], указывающий на то, что изменение химической природы поверхности адсорбента путем проведения химических реакций приводит к изменению адсорбционной активности не только веществ, адсорбция которых является результатом электростатического взаимодействия, но и веществ, адсорбирующихся только в результате дисперсионного взаимодействия. Так, по мере замещения поверхностных гидроксильных групп силикагеля органическими радикалами или атомами фтора адсорбция паров как полярных, так и неполярных веществ уменьшается. Наиболее сильно это уменьшение выражено для паров воды, спиртов, в меньшей мере - для паров бензола и еще в меньшей степени для азота и аргона. [13]
Кремнеземы с гидроксилированной поверхностью специфически адсорбируют молекулы, относящиеся к группам В и D. Вместе с тем благодаря слабо кислому характеру силанольных гадроксильных групп на поверхности чистых образцов кремнезема передачи протона на адсорбированные молекулы обычно не происходит. Взаимодействие ограничивается образованием с молекулами групп В и D водородных связей. Для снижения специфичности молекулярных адсорбционных взаимодействий обычно проводятся реакции деги-дроксидирования ( при нагревании в вакууме до 1000 концентрация гидроксильных групп на поверхности аэросила уменьшается приблизительно на порядок [21, 26]) или реакции замещения поверхностных гидроксильных групп на алкилсилильные или ал-коксильные радикалы. [14]
Страницы: 1