Положительная валентность
Cтраница 2
Сумма единиц положительной валентности должна быть равна сумме единиц отрицательной валентности. Деля 10 на число единиц положительной валентности фосфора 5, узнаем что фосфора содержится в молекуле 2 атома. [16]
Сумма единиц положительной валентности должна быть равна сумме единиц отрицательной валентности. [17]
Помимо величины положительной валентности, на характер оксида и гидроксида влияет радиус центрального атома. Рассмотрим изменение характера оксидов и гидроксидов по подгруппам элементов. [18]
Высшее значение положительной валентности, равное для элементов коротких периодов числу электронов во внешней оболочке, нарастает от 1 до 7, но оно не может проявляться у кислорода и фтора как наиболее электроотрицательных элементов, неспособных отдавать электроны. [19]
Из 4 положительных валентностей водородных атомов 3 нейтрализуют 3 отрицательные валентности азота. Четвертая валентность составляет положительный заряд иона. [20]
Металлы проявляют положительную валентность, так как атомы металлов теряют свои электроны. Неметаллы могут проявлять как положительную, так и отрицательную валентность, так как атомы неметаллов, в зависимости от условий реакции, могут либо терять, либо присоединять электроны. Но наиболее характерным для неметаллов является образование ионов, связанное с приобретением электронов. [21]
Металлы проявляют положительную валентность, так как атомы металлов теряют свои электроны. Неметаллы могут проявлять как положительную, так и отрицательную валентность, так как атомы неметаллов, в зависимости от условий реакции, могут либо терять, либо присоединять электроны. Для неметаллов наиболее характерно образование ионов, связанное с потерей электронов. [22]
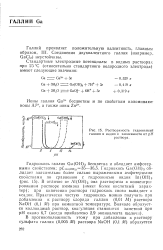 |
Растворимость гидроокисей. [23] |
Галлий проявляет положительную валентность, главным образом, III. Соединения двухвалентного галлия ( например, GaCb) неустойчивы. [24]
Металлы проявляют исключительно положительную валентность. Для неметаллов характерна отрицательная валентность, которая вызвана присоединением электронов, доведением числа валентных электронов до октета. [25]
Металлы проявляют только положительную валентность. Величина положительной валентности равна количеству электронов, которые отдает атом. [26]
Литий проявляет положительную валентность I. Такое низкое значение потенциала, вероятно, связано с сильной гидратацией ионов лития в водных растворах. Выделить литий электролизом водных растворов невозможно. [27]
Торий проявляет положительную валентность IV. Соединения тория более низкой валентности неустойчивы в водных растворах. [28]
Титан проявляет положительную валентность IV, III и II. Соединения трехвалентного титана легко окисляются кислородом воздуха. [29]
Рений проявляет положительную валентность III, IV, V, VI и VII. Для аналитической химии наибольшее значение имеют соединения рения в семивалентном ( перренаты) и четырехвалентном состояниях. Валентность рения во многих соединениях, образующихся при взаимодействии перрената калия с аналитическими реагентами, достоверно не установлена. [30]
Страницы: 1 2 3 4