Затвердевание - система
Cтраница 1
 |
Диаграмма состояния двойных. [1] |
Затвердевание системы АтВ - 54 ся по линии C - этом по линии Ci таллизуется химическое соединение АтВп, а по линии E2Bi чистый компонент В. [2]
 |
Диаграмма состояния двойных. [3] |
Затвердевание системы Л - АтВп происходит по линии А Е С1 По линии А1Е1 кристаллизуется компонент Л, а по линии Е1 С1 химическое соединение АтВп. Окончательное затвердевание сплава происходит при эвтектической температуре по линии DiEfi. В точке Ег одновременно кристаллизуются Л и АтВп. Сплав такого состава после затвердевания имеет эвтектическое строение. [4]
Затвердевание системы в концентрационном интервале, определяемом эвтектической линией GH, всегда связано с достижением эвтектического состояния. Если состав исходной жидкости находится в границах концентраций от точки К до чистого компонента А или от точки М до чистого компонента В, то в процессе охлаждения будут выделяться только кристаллы а - или р-фазы. [5]
Мы там рассмотрели процесс затвердевания системы с фигуративной точкой F: эта точка лежит в поле компонента Лив треугольнике АЕЕ, и действительно процесс затвердевания этой системы начинается кристаллизацией компонента А, затем следует совместная кристаллизация А и В и, наконец - совместная кристаллизация А, В и С. [6]
Была исследована зависимость температуры затвердевания бинарных спиртовых систем от состава последних. [7]
Необходимо отметить, что при затвердевании систем, в которых не образуется твердых соединений между компонентами расплава и газом, растворенные в них газы выделяются. В зависимости от того, происходит ли химическое взаимодействие между растворителем и растворенным веществом или оно отсутствует, растворы газов в расплавленных солях можно разбить на две группы. [8]
Для существенного упрощения записи уравнений в ряде случаев используется принцип затвердевания системы. [9]
Рассмотрим другой вид уравнения Лагранжа второго рода для переменных масс с применением принципа затвердевания системы. Покажем, как в данном случае применение этого принципа избавляет от утомительных вычислений, связанных с составлением уравнений движения. [10]
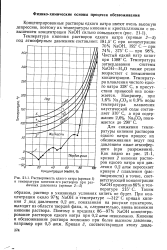 |
Растворимость едкого натра ( кривая / и температуры кипения его растворов при различных давлениях ( кривые 2 - 5. [11] |
Чистый едкий натр кипит при 1388 С. Температура затвердевания системы NaOH - Н2О также резко возрастает с повышением концентрации. Температура плавления чистого едкого натра 328 С, в присутствии примесей она понижается. Например, при 1 6 % Na2CO3 и 0 9 % воды температура плавления каустической соды составляет 310 С, а при содержании 2 6 % Na2CO3 понижается до 290 С. [12]
Ниже определенной критической температуры - точки замерзания - вода существует как твердое тело. Аналогично затвердеванию систем, построенных на липидной основе, например мембран, замерзание воды часто бывает неблагоприятно для жизни, особенно если образование льда происходит внутри клетки. [13]
Как следует из данных табл. 1.22, не все реакции фазообра-зования сопровождаются контракцией. Типичным случаем является затвердевание системы Са ( ОН) 2 - SiO2 - Н2О при высокой температуре, когда образуется ксонотлит. [14]
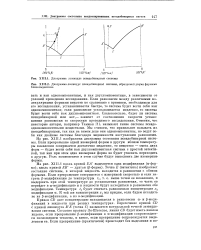 |
Диаграмма ликвидус псевдобинарной системы.| Диаграмма ликвидус псевдобинарной системы, образуемой двумя формами. бензальдоксима. [15] |
Страницы: 1 2