Анодная защита - титан
Cтраница 1
Анодная защита титана может быть использована в серной кислоте концентрацией до 60 % при 60 С и до 40 % при 90 С; в 60 % - ной фосфорной и 37 % - ной соляной кислотах - до 60 С; в муравьиной кислоте, из которой удален воздух - до точки кипения; в 25 % - ной щавелевой - до 90 С и в 20 % - ной сульфаминовой - до 90 С. [1]
Впервые эффективность анодной защиты титана в серной кислоте была показана Коттоном на модельной установке [84], в которой рециркулировала 40 % - ная серная кислота при 60 С. [2]
Зорченко и И. П. Анощепко [23] предложили для анодной защиты титана в серной кислоте протекторы из сурьмы и висмута. [3]
Интересная работа выполнена коллективом авторов [87], изучавших возможность анодной защиты титана при получении хлората хрома, основанном на растворении его гидрокси-да соляной кислотой. При введении в раствор совместно с хлоратом хлорида хрома ( сильного восстановителя) стационарный потенциал титана сдвигается в сторону отрицательных значений от 0 6 до - 0 12 В. [4]
АН СССР, 1958, 121, № 5, 885; Анодная защита титана в серной и соляной кислотах. [5]
 |
Зависимость времени эффективной обработки графитового протектора от защитной плотности тока. [6] |
Таким образом, предварительно окисленный в серной кислоте графитовый электрод можно эффективно использовать в качестве катодного протектора при анодной защите титана в соляной кислоте в широком интервале концентраций и температур. [7]
А л ь т о в с к и и, А р а к е л о в, Анодная защита титана в серной и соляной кислотах. [8]
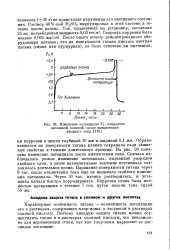 |
Изменение потенциала Ti, покрытого. [9] |
Поэтому анодную защиту титана можно осуществлять также и в растворах соляной кислоты, что невозможно для нержавеющей стали, так как хлор-ионы нарушают ее пассивное состояние. [10]
Очевидно, что проводить анодную защиту при потенциалах, более положительных, чем этот потенциал, нецелесообразно, потому что при этом будет бесполезно расходоваться электроэнергия на протекание побочного анодного процесса. При анодной защите титана в соляной кислоте сильное смещение потенциала в положительную сторону является не только нецелесообразным из-за излишнего расхода тока, но и опасным, поскольку это может привести к пробиванию анодной окисной пленки ионами хлора и, следовательно, к нарушению пассивного состояния-и развитию питтинговой коррозии. [11]
При увеличении поверхности титана, находящегося в объеме кислоты, сверх критического соогношения, не только не происходит его активация, но и прекращается щелевая коррозия. Возникает съоего рода анодная защита титана в зазоре. [12]
 |
Скорость коррозии титана в контакте. [13] |
При более длительных ( 10-часовых) испытаниях скорость коррозии анодно защищаемого титана снижается примерно в 10 раз и составляет около 0 085 г / м2 - ч, или 0 16 мм / год. Эти довольно низкие значения скорости коррозии указывают на практическую возможность анодной защиты титана в кипящей 40 % - ной серной кислоте. Различия, полученные в наших опытах и опытах Коттона, скорее всего являются следствием использования титана различного качества, что, в свою очередь, могло влиять на защитные свойства окисных пленок, образующихся при анодной поляризации. [14]
Таким образом, пробой анодной пленки и развитие питтинговой коррозии на титане в растворах хлоридов средней концентрации практически могут осуществляться в результате воздействия внешнего анодного тока, при наложении которого достигаются любые положительные потенциалы. Необходимо также учитывать опасность пробивания анодной пленки галоидными ионами при осуществлении анодной защиты титана в кислых средах, содержащих ионы галоидов. В этом случае необходимы строгий контроль за потенциалом защищаемой конструкции и автоматическое его регулирование с целью поддержания потенциалов в безопасной области. [15]
Страницы: 1 2