Значение - потенциал
Cтраница 4
Значение потенциала на электроде ( Vw) при высокой проводимости последнего практически постоянно. [46]
Значение потенциала, при котором прекращается коррозионный процесс, называется защитным потенциалом, а плотность тока, обеспечивающая сдвиг потенциала до защитного - защитная плотность тока. [47]
Значения потенциалов, соответствующие плато на кривых Е - t, и отвечают, очевидно, максимальным различиям в активностях комплексона в поверхностных слоях мембраны, находящихся в контакте с растворами КС1, значительно различающимися по концентрации. Диффузия комплексона ведет к выравниванию этих активностей, вследствие чего уменьшается значение последнего интеграла в уравнении ( 5) и происходит рост потенциала электрода. [48]
Значения потенциалов для этих реакций получены расчетным путем. Их скорость определяется концентрацией ионов М - 2 и Mg в электролите. [49]
Значения потенциалов приведены по отношению к нормальному водородному электроду. [51]
Значение потенциала можно легко сдвинуть, изменяя кислотность среды, хотя возможности смещения его в отрицательную область ( большие значения рН) ограничены образованием осадков гидроксидов выделяемых катионов. Сильно отрицательное перенапряжение водорода ( г ] Н2) на многих металлах по этой причине оказывает благоприятное влияние, поскольку дает возможность проводить электрогравиметрическое определение ряда металлов, как было указано выше. Наконец, следует также учитывать, что потенциал водорода в процессе электролиза сдвигается в сторону положительных значений, так как в растворе возрастает концентрация ионов Н3О, образующихся эквивалентно количеству выделившегося на катоде металла. Потенциал выделения водорода и по окончании электролиза не должен достигать потенциала зоны осаждения. [52]
Значения потенциалов даны относительно водородного электрода. [53]
Значения потенциалов в тексте, таблицах и графиках приводятся в пересчете на нормальный водородный электрод. [54]
Значение потенциала в растворе, в котором концентрация окислительной формы равна концентрации восстановленной, называется нормальным окислительно-восстановительным потенциалом. [55]
Значения потенциалов даны относительно водородного электрода в том же растворе. Наиболее активный электрод получен при использовании в качестве носителя угля БАУ. Несколько большая поляризуемость ( приблизительно на 100 мВ) имеет место для носителей из ацетиленовой сажи и активированного угля КАД-молотый. [56]
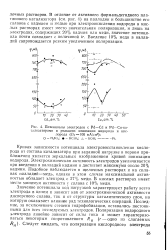 |
Потенциалы электродов с Pd - Cd и Pd - Cu-ка-талпзаторами в реакциях ионизации водорода и кис. [57] |
Значение потенциала под нагрузкой характеризует работу всего электрода в целом и зависит как от электрохимической активности дисперсного сплава, так и от структуры каталитического слоя, на которую оказывает влияние ряд технологических операций. Последние, за исключением степени гидрофобизации, оставались постоянными для всех исследуемых электродов. [58]
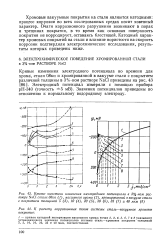
Значение потенциала, равное - 0 85 В, выбрано и используется специалистами в качестве базового для сравнения на том основании, что поляризация стальных конструкций до указанного значения ( U - - 0 85 В) относительно медно-сульфатного ( Cu / CuSO4) электрода и его стабильное поддержание на таком уровне обеспечивают полную защиту стали от коррозии. Этот параметр, эмпирически установленный в 1928 г. и подтвержденный в дальнейшем многолетними наблюдениями, в настоящее время является повсеместно принятым критерием катодной защиты стали. [59]
Значения потенциалов приводятся с точностью до третьей значащей цифры. Значком отмечены ненадежные цифры. [60]
Страницы: 1 2 3 4