Аналог - сера
Cтраница 2
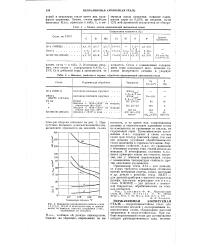 |
Изменение механических свойств стали с 0 11 % С, 13 % Сг и присадкой серы в зависимости от темп-ры отпуска ( выдержка 5 час., охлаждение на воздухе. [16] |
Хромоникелевые аусте-нитные А.н.с. содержат в своем составе селен или теллур ( аналоги серы), так как эти добавки улучшают обрабатываемость стали давлением в горячем состоянии. Коррозионная стойкость А.н.с. по сравнению с обычными сортами этих сталей несколько меньшая. В атмосферных условиях А.н.с. имеет примерно такую же скорость коррозии, как у обычной нержавеющей стали; с повышением температуры стойкость против окисления ухудшается. [17]
Если соблюдать принцип нарастания атомного веса чисто формально, то йод оказался бы аналогом серы, а теллур - аналогом брома. [18]
Менделеев все время предупреждает химиков, что нельзя отрывать качество от количества. Хотя типы соединений, образуемых аналогами серы и фосфора, различны - пишет он - однако нельзя не видеть огромного сходства, существующего между серой и фосфором, а в особенности между мышьяком и селеном и, еще более, между теллуром и сурьмою. Группируя элементы по качеству их соединений и не обращая притом внимания на атомный состав соединений, мы должны были бы ближе всего считать именно эти два элемента. Это различие четности и нечетности хлоров, содержащихся в типических соединениях данного элемента, выставляется нередко как важнейший характер элемента. Но мы уже знаем примеры, что один и тот же элемент дает соединения четных и нечетных типов ( наприм. NO относятся к типу NX и NX2, так же как CuCl и CuCi2), а впоследствии мы познакомимся еще с большим числом таких соединений; а потому явственное сходство нельзя видеть в одном сходстве типов, образуемых данными элементами. Хотя теллур и сурьма образуют соединения разных типов, но они и в свободном состоянии, и в форме своих окисей, и в соединении с водородом и хлором, словом во всем своем химическом характере представляют высшую ступень качественного сходства. [19]
В стекольном производстве теллуром пользуются, чтобы придать стеклу коричневую окраску и больший коэффициент лучепреломления. В резиновой промышленности его, как аналог серы, иногда применяют для вулканизации каучуков. [20]
Формулы солеобразую-щих окислов ( гл. Уран, перенесенный из группы железа в аналоги серы ( гл. Индий и впервые об элементах с атомн. [21]
Как было показано ранее, соединения с высшим числом частиц воды встречаются сравнительно редко и притом главным образом среди галоидных солей первой группы периодической системы, Такие соединения Ф. М. Флавицкий называет гидратами высшего порядка и принимает, что при образовании их участвует кислород с атомностью выше двух, как это обыкновенно принимается. Согласно своему положению в периодической системе, кислород как аналог серы должен быть шестиатомным элементом. При таком воззрении вода представляется ненасыщенным телом, и на-каждый атом кислорода в гидро-орто-форме и ее производных могут присоединиться по крайней мере две частицы воды. В связи с этим мы должны учесть то обстоятельство, что более богатые кислородом остатки йодной, серной и других кислот оказываются в то же время способными удерживать наибольшее число частиц воды, которое значительно превышает содержание последней в орто-формах. [22]
Крукс полагал, что эта пыль должна содержать селен и теллур, аналоги серы. [23]
Переход электронов с одного уровня на другой становится тем более вероятным, чем дальше от ядра расположены валентные электроны и чем энергетически ближе к основному состоянию оказываются незанятые уровни. Этим объясняется валентность 6 у серы ( SFe), 7 - у иода ( IF7), 8 - у осмия ( OsF8) и отсутствие такой высокой валентности у кислорода, фтора, железа, аналогов серы, иода и осмия, расположенных в периодической системе выше. [24]
Переход электронов с одного уровня на другой становится тем более вероятным, чем дальше от ядра расположены валентные электроны и чем энергетически ближе к основному состояния оказываются незанятые уровни. Этим объясняется ковалентность 6 у серы ( SF6), 7 - у иода ( IF7), 8 - у осмия ( OsF8) и отсутствие такой высокой ковалентности у кислорода, фтора, железа, аналогов серы, иода и осмия, расположенных в периодической системе элементов выше. Необходимость больших энергетических затрат на возбу / кдение атомов гелия, неона и аргона и невозможность их компенсации объясняют инертность этих элементов, хотя для их аналогов - криптона, ксенона и радона - получены соединения с ко-валентностыо 2, 4, 6 и 8 ( KrF2, KjF. [25]
Но иногда этот элемент, а в еще большей мере некоторые его соединения прибавляют врачам хлопот. Из соединений теллура самое опасное - теллуроводоред Н 2Те, бесцветный ядовитый газ с неприятным запахом. Последнее вполне естественно: теллур - аналог серы, значит, Н2Те должен быть подобен сероводороду. Он раздражает бронхи, вредно влияет на нервную систему. [26]
Соединения серы с углеводородными остатками входят в I блок органических соединений атомов органогенов. Ранее уже кратко упоминалось о соединениях Se и Те. Здесь следует добавить, что для селена типичны аналоги серы RSeH, R2Se, RSe-SeR и R-Se - - Cl. Они получаются так же, как и соединения с серой. [27]
Она существует лишь при охлаждении до - 80; при повышении температуры она через несколько секунд переходит в желтую а-серу. Другую аллотропическую модификацию - ромбоэдрическую серу, кристаллы которой построены из молекул S6, можно получить, извлекая серу толуолом из ее подкисленного раствора в гипосульфите. Еще одна новая модификация серы, состоящая, вероятно, из линейных молекул S8, получена при конденсации в вакууме паров серы на поверхности, охлажденной жидким азотом. Эта аллотропическая модификация - аналог пурпурной серы, но при ее получении конденсируемые пары могут быть нагреты сравнительно невысоко. [28]
Крукс [385, 388], наблюдая в 1861 г. спектр шламма сернокислотного производства, заметил в нем зеленую линию ( X 535 ммк), не соответствовавшую ни одному из ранее известных элементов. При исследовании этого вещества был обнаружен новый элемент. Дата опубликования первой статьи о таллии - 30 марта 1861 г. - считается днем открытия этого элемента. Крукс вначале ошибочно принял таллий за металлоид, аналог серы, селена и теллура. [29]
Для горячей вулканизации ( см.) к резине примешивают с е р у в количестве 3 - 12 вес. Применение сильных ускорителей вулканизапии дает возможность уменьшать количество серы до 2 - - 2 5 вес. Для дешевых малоответственных сортов резины обычно применяется молотая сера. Для высших сортов резины берется серный цвет; применение его обязательно для резины, идущей на изготовление клеев, вследствие его малой растворимости в бензине и отсутствия поэтому выкристаллизовывания серы при испарении бензина из клея. В сортах резины, в к-рых не допускается попадания посторонних включений, применяется осажденная сера, однако она часто выцветает-выступает на поверхность ( см. Рыцветание серы), затрудняя некоторые производственные операции. Аналог серы, селен, также изредка применяется в качестве вулканизующего агента; вследствие его высокой t njl. При этом после вулканизапии получается плгтная резина, хорошо сопротивляющаяся истиранию. Хлористая сера 82С ] 2 применяется для холодной вулканизации. [30]
Страницы: 1 2 3