Извлечение - сернистый ангидрид
Cтраница 2
Значительный интерес представляют возможности извлечения сернистого ангидрида из газов непосредственно в самом котлоагрегате. [16]
Весьма перспективен циклический магнезитовый метод извлечения сернистого ангидрида из малоконцентрированных газов. [17]
В третью группу процессов очистки газов от сернистого ангидрида входят процессы, в которых извлечение сернистого ангидрида осуществляется совместно с его использованием для получения новых химических веществ. Эта группа процессов характеризуется тем, что поглотитель в процесс не возвращается, а используется для реакции с сернистым ангидридом. [18]
Все процессы целесообразно прежде всего разделить на два основных класса, отличающихся по физическому состоянию применяемого основного реагента для извлечения сернистого ангидрида из газов. [19]
Некоторые методы ( магнезитовый, содо-цинковый и др.) при их применении на предприятиях цветной металлургии и химической промышленности позволяют сочетать извлечение сернистого ангидрида с его утилизацией для получения серной кислоты. [20]
Дымовые газы, выделяющиеся при сжигании сернистых углей на силовых станциях, содержат от 0 3 до 0 6 % SO2, и извлечение сернистого ангидрида является трудной задачей, связанной с необходимостью обработки больших количеств запыленных газов, имеющих высокую температуру и влажность. До настоящего времени в лабораторном масштабе и на опытных установках не найдено удовлетворительного решения этой задачи. [21]
Основные меры по сокращению выбросов в атмосферу окислов серы в 1981 - 1985 гг. будут приниматься в двух основных направлениях - снижение сернистости потребляемого топлива и сооружение опытно-промышленных установок по извлечению сернистого ангидрида - из дымовых газов на выходе из котлоагрегатов. [22]
Сернистый ангидрид, содержащийся в относительно небольших концентрациях в отходящих газах промышленных предприятий, является основным источником загрязнения воздушного бассейна. Поэтому проблема санитарной охраны чистоты воздуха - это прежде всего проблема извлечения сернистого ангидрида из так называемых бедных сернистых газов, выпускаемых в атмосферу. [23]
С, что связано с образованием углекислой соли. При повышении температуры до 700 - 800 С, когда скорость образования углекислых солей уменьшается ввиду приближения к температуре диссоциации ( 900 С), извлечение сернистого ангидрида происходит полнее, но в течение более длительного периода. [25]
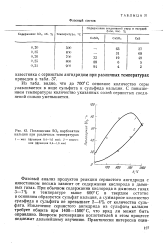 |
Поглощение SOa карбонатом кальция при различных температурах. [26] |
Фазовый анализ продуктов реакции сернистого ангидрида с известняком весьма зависит от содержания кислорода в дымовых газах. При обычном содержании кислорода в дымовых газах 3 - 7 % и температуре выше 600 С в твердом остатке в основном образуется сульфат кальция, а суммарное количество сульфида и сульфита не превышает 2 - 4 % от количества сульфата. Извлечение сернистого ангидрида из сульфата кальция требует обжига при 1400 - 1500 С, что вряд ли может быть оправдано. [27]
Пробу необходимо тонко измельчить, равномерно, тонким слоем распределить на дне лодочки для сжигания и покрыть слоем флюса. Кислород и аргон перед подачей в печь для сжигания пропускают сначала над платинированным асбестом при 450 С для окисления присутствующих углеводородов, затем черев карбосорб и ангидрон для извлечения двуокиси углерода и воды. Газы, выходящие из печи для сжигания, проходят через ангидрон для удаления воды, затем через двуокись марганца для извлечения сернистого ангидрида. При анализе титановой губки или гранул, содержащих хлориды магния и натрия, для извлечения хлора необходима еще одна ловушка с асбестом, покрытым безводным сульфатом меди. [28]
 |
Газовый абсорбер ( А с регенерацией абсорбента путем отдувки острым паром в дистилляционной колонне ( B. [29] |
Важным примером этого служит применение водных растворов этаноламинов для абсорбции диоксида углерода в производстве водорода. Эти растворы образуют непрочные химические соединения с СО2, которые можно разрушать нагреванием или уменьшением давления, для освобождения диоксида углерода и повторного использования растворителя. На рис. 11.1 показано применяемое для той же цели устройство в виде блока абсорбера и дистилляционной колонны. Аналогичная система действует при применении регенерируемого абсорбента для извлечения сернистого ангидрида из топочных газов электростанций и хвостовых газов установок Клауса путем организации работы абсорбера и десорбера при разных давлениях или температурах. В случае эксплуатации при различных давлениях абсорбер работает при значительно большем давлении, чем давление в десорбере, но практически при такой же самой температуре. При температурном перепаде давления в обоих аппаратах приблизительно одинаковы, но абсорбер действует при более низкой температуре, чем де-сорбер. [30]
Страницы: 1 2 3