Извлечение - растворенное вещество
Cтраница 2
Теория извлечения учит, что извлечение растворенного вещества определенным количеством растворителя удается тем совершеннее, чем на большее число фракций разделен растворитель. Однако для извлечения из органических растворов с помощью воды, щелочей и кислот другого пути не существует. При этом часто нужно иметь в виду, что многие соли органических кислот плохо растворимы в щелочных растворах. Следовательно, сначала нужно извлекать не только небольшими количествами, но также и применять меньшие концентрации щелочей, и лишь позднее повышать их. [16]
Такие уравнения преобразования получены для процессов извлечения растворенного вещества из пористых тел. [17]
Закон распределения успешно применяется в практике извлечения растворенного вещества из раствора с помощью другого растворителя. С его помощью возможно производить расчеты количества извлекаемого вещества и наиболее эффективные варианты процесса экстракции. [18]
Уравнения (2.36) и (2.37) справедливы как при извлечении растворенного вещества, так и при извлечении твердого вещества. Соответствующие значения Ху определяются в разделе 1.1. В уравнениях (2.36) и (2.37) N - число частиц в единице объема слоя, R - радиус частицы. [19]
Экстрагирование ( экстракция) - это довольно распространенный метод извлечения растворенного вещества путем взбалтывания с другим несмешивающимся растворителем, в котором данное вещество растворяется гораздо лучше. Процесс экстракции ускоряется при увеличении поверхности между фазами, что достигается перемешиванием, измельчением твердых веществ и другими приемами. [20]
Экстрагирование ( экстракция) - это довольно распространенный метод извлечения растворенного вещества путем взбалтывания с другим несмешивающимся растворителем, в котором данное вещество растворяется гораздо лучше. Процесс экстракции ускоряется при увеличении поверхности между фазами, что достигается перемешиванием, измельчением твердых веществ и другими приемами. [21]
Экстрагирование ( экстракция) - это довольно распространенный метод извлечения растворенного вещества путем взбалтывания с другим несмешивающимся растворителем, в котором данное вещество растворяется гораздо лучше. Процесс экстракции ускоряется при увеличении поверхности раздела между фазами, что достигается перемешиванием, измельчением твердых веществ и Другими приемами. [22]
 |
Распределение иода в воде и сернистом углероде.| Распределение брома в воде и сернистом углероде. [23] |
Эту закономерность используют в промышленности и в аналитической химии для извлечения растворенного вещества из раствора путем применения другого растворителя, в котором данное вещество лучше растворяется. [24]
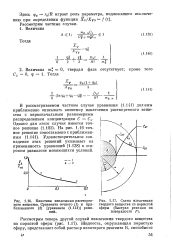 |
Кинетика извлечения растворенного вещества. Сравнение точного ( 1 и приближенного ( 2 [ уравнение ] решений.| Схема извлечения. [25] |
В рассматриваемом частном случае уравнения (1.141) должны приближенно описывать кинетику извлечения растворенного вещества с первоначальным равномерным распределением концентрации С Cs. Удовлетворительное совпадение этих решений указывает на применимость уравнений (1.138) в широком диапазоне меняющихся условий. [26]
 |
Доли растворенного вещества в различных фазах при противоточном распределении. [27] |
Верхние и нижние фазы в экстракционных трубках объединяют для анализа или извлечения растворенного вещества. Таким образом, представляет интерес расчет суммарной доли растворенного вещества в каждой трубке. [28]
 |
Кривые растворимости различных солей. [29] |
Закон распределения широко используют при экстрагировании, подбирая более выгодные условия извлечения растворенного вещества. [30]
Страницы: 1 2 3 4