Анетол
Cтраница 2
Пропенилфенилметиловый эфир ( анетол) имеет слабое антисептическое действие. Присутствие свободной гидроксильной группы, например в эвгеноле, повышает антисептическую и наркотическую активность, а токсичность уменьшается приблизительно на одну треть. Метыленовые эфиры типа сафрола ( 4-аллил-метилен - диоксибензола) являются более сильными наркотиками, чем эвгенол, но их местное раздражающее действие слабее, чем у анетола. Изосафрол менее активен как наркотик, чем сафрол; возможно, что это связано с большей устойчивостью алкильного радикала. Такие же отношения существуют и между апиолами. Кубебин, который имеет в алкильном радикале гидроксил, физиологически почти неактивен. [16]
Превращение мотилхавикола в анетол происходит, по Ж - Эик-маиу [1438], при простом кипячении этого соединения с раствором едкого кали и этиловом спирте; реакция эта является общей для всех аллильных производных бензола вообще. Сам аллилбеизол, согласно Клагесу [1439], превращается при нагревании со спиртовым раствором едкого кали в запаянной трубке. [17]
Побочная реакция окисления анетола с образованием анисовой кислоты подавляется прибавлением сульфанилата натрия. По окончании реакции отделяют толуольный экстракт, отгоняют толуол и технический обепин перегоняют в вакууме в присутствии гидрокарбоната натрия. [18]
При нитровании - анетола гексанитроэтаном по прописи Шмидта в присутствии пиридина и сухого эфира при 0 С был выделен р-нитроанетол, правда с меньшим выходом, чем при применении тетранитрометана. Нитрование тетранитрометаном арилалкенов в среде спирта приводит к образованию а-алкокси-р-нитросоеди - нений. [19]
Отсутствие показателя содержание анетола во многих национальных нормативно-технических документах связано с зависимостью температуры застывания от содержания анетола. Это видно из следующих данных, рекомендуемых для расчетов. [20]
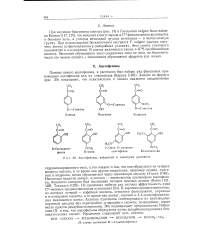 |
Ацетофеноны, найденные в некоторых растениях. [21] |
При изучении биосинтеза анетола ( рис. 19) в Foeniculum vulgare было найдено Канеко [117, 119], что меченый атом углерода а - С14 - фенилаланина включается в боковую цепь, а углерод метильной группы метионина - в метоксильную группу. [22]
В состав масла входят анетол ( более 85 %), метилхавикол ( около 10 %), а-фелландрен, лимонен, дипентен, а-пинен, камфсн, р-фарнезен, у-гимахалсн, куркумсн, анисовый альдегид, анискетон, гидрохинон и его монометиловый эфир, и-крезол, пропионовая, масляная, миристиновая и анисовая кислоты, серосодержащие соединения и другие компоненты. [23]
В состав масла входят анетол ( более 80 %), фенхон ( до 25 %), транс -, цис - и транс, / п / игис-аллооцимены, мирцен, а - и у-терпинены, дипентен, фелландрены, а - и ( 3-пинены, камфен, 3-карен, сабинен; я-цимол, мстилхавикол и др. компоненты. [24]
Подходящими растворителями являются также анетол, пиридин и ксилол. [25]
Анизол образуется при расщеплении анетола ( стр. Применяется анизол в качестве растворителя и исходного вещества для некоторых синтезов, например при получении n - метоксиацетофенона СНзОСеЬЦСОСНз, являющегося душистым веществом. [26]
При попытке осуществить деметилирование анетола с помощью спиртового едкого кали в запаянной трубке Доддсу и Лоусону удалось выделить лишь сырой маслянистый препарат анола, который и был испытан на биологическую активность. [27]
Выделенный нами продукт роданирования анетола содержал азот в количестве, соответствующем продукту присоединения. [28]
При насыщении эфирного раствора анетола окислами азота при ильном охлаждении, так же как и при прибавлении раствора азотистокислого натрия к анетолу, растворенному в ледяной уксусной кислоте ( способы Тенниса и Анджели), образуется а н е т о л-псевдонитрозит, который при кипячении со спиртом превращается в анизилнитроэтилкетоксим. [29]
При реакции серы с анетолом, кроме того, выделено соединение C2oH2oO2S ( выход 20 %), по-видимому, являющееся соответствующим производным тиофена, а также незначительное количество соединения C20Hi9O2S2, вероятно, содержащее два конденсированных тиофеновых ядра. [30]
Страницы: 1 2 3 4