Излом - кондуктометрическая кривая
Cтраница 1
 |
Кривые комплексонометрического титрования. [1] |
Излом кондуктометрической кривой в точке эквивалентности объясняется ростом концентрации ионов натрия за счет диссоциации избытка натриевой соли ЭДТА. [2]
В случае, когда излом кондуктометрической кривой вблизи точки эквивалентности закруглен, для установления точки эквивалентности используют участки кривой, достаточно удаленные от нее. [3]
 |
Ковдуктометрические кривые титрования при использовании реакции осаждения, окисления - восстановления и комплексообразования. [4] |
При кондуктометрическом титровании необходимо, прежде всего, чтобы излом кондуктометрической кривой позволял устанавливать точку эквивалентности с достаточной точностью. [5]
Реакция нейтрализации кислоты до Na3PO4 сильно обратима, и излом кондуктометрической кривой, фиксирующий полную нейтрализацию кислоты, не обнаруживается. Поэтому кондуктометрическое определение фосфорной кислоты основывается на нейтрализации первого кислотного эквивалента. [6]
Таким образом, подвижности ионов оказывают существенное влияние на формы кривых кондуктометрического титрования и величину угла излома кондуктометрической кривой в точке эквивалентности. [7]
Точки эквивалентности на кондуктометрических кривых устанавливают графическим методом и находят число интервалов между показаниями милливольтметра до изломов кондуктометрических кривых. При этом в расчетную формулу вводят число интервалов, соответствующих титрованию отдельных кислот. Грамм-эквивалент аминоуксусной кислоты принимают равным ее мольной массе. [8]
На кривых титрования графическим методом устанавливают точки эквивалентности и определяют число интервалов между записями показаний милливольтметра до изломов кондуктометрических кривых. [9]
При титровании сильными кислотами щелочных растворов амфолита сначала вытесняются слабые кислотные группы, а затем нейтрализуются основные группы, что сопровождается изломами кондуктометрических кривых. Если ( рА а рКъ) 12 - 4 - 16, обе реакции протекают параллельно и кондуктометрические кривые имеют один излом, соответствующий окончанию обеих реакций. [10]
Нелинейное изменение электропроводности раствора при титровании нередко наблюдается даже в том случае, когда реакция протекает количественно. Излом кондуктометрической кривой при этом в точке эквивалентности может быть резким, но сама Кондуктометрическая кривая имеет различные особенности ( изогнутость, пологий минимум или максимум), которые не имеют аналитического значения. [11]
Кондуктометрическую кривую строят, откладывая по оси абсцисс число миллилитров добавленного титранта, а по оси ординат - электропроводность раствора, приведенную к первоначальному объему. Затем графическим методом по излому кондуктометрических кривых устанавливают точку эквивалентности и определяют число миллилитров стандартного раствора, вступившего в реакцию. [12]
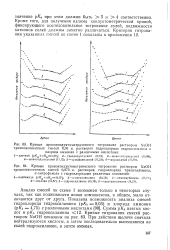 |
Кривые хронокондуктометрического титрования раствором NaOH трехкомпонентных смесей 0 05 н. растворов гидрохлорида гидроксиламина и.| Кривые хронокондуктометрического титрования раствором NaOH. [13] |
Кроме того, для получения излома кондуктометрической кривой, фиксирующего последовательное титрование солей, подвижности катионов солей должны заметно различаться. [14]
Для осаждения бензоат-ионов используют перхлорат ртути. Вследствие некоторой растворимости осадка бензоата ртути излом кондуктометрической кривой в точке - эквивалентности закруглен. [15]
Страницы: 1 2 3