Измерение - электродный потенциал
Cтраница 1
 |
Лабораторный рН - метр типа ЛП-58. [1] |
Измерение электродного потенциала или разности потенциалов - непростая задача. [2]
Измерение электродных потенциалов в водопроводной воде показало, что более грубой обработке поверхности соответствует более отрицательное значение начального электродного потенциала. [3]
Измерение электродных потенциалов и снятие поляризационных кривых проведено в дистиллированной воде на образцах размером 10x10 мм. [5]
Измерение электродных потенциалов лежит в основе потен-циометрии. В зависимости от типа используемых при титровании реакций различают потенциометрическое титрование по методу осаждения, комплексообразования, нейтрализации и окислительно-восстановительное потенциометрическое титрование. В первых двух разновидностях потенциометрического титрования используют электроды, обратимые по отношению к ионам, которые входят в состав осадка или комплексного соединения. Потенциал таких электродов определяют относительно какого-либо электрода сравнения в ходе постепенного добавления титранта. Потенциометрическое титрование, например, очень удобно для определения анионов, образующих нерастворимые соли с ионом серебра. При этом часто в качестве индикаторного используют серебряный электрод. [6]
Измерение электродного потенциала осуществляют с помощью систем, состоящих из двух электродов. Один из них - индикаторный ( стеклянный, платиновый) электрод - чувствителен к ионам, присутствующим в растворе, и потенциал, возникающий на кем, зависит от концентрации ионов в испытуемом растворе. Другой электрод - электрод сравнения ( каломельный или хлорсеребряный) - не чувствителен к ионам раствора, потенциал его постоянен. [7]
 |
Схема элемента Вестона. [8] |
Измерение электродных потенциалов ( потенциометрия) используется также для определения концентрации кислот и щелочей, растворимости малорастворимых веществ, позволяет рассчитать константу равновесия химической реакции, коэффициент активности в растворах электролитов. [9]
 |
Способы крепления ( а, б и армирования образцов ( в, г для измерения электродных потенциалов. [10] |
Измерение электродных потенциалов используется непосредственно, а также применяется в других методах. [11]
Измерения электродных потенциалов [53] показали, что упрочненный светлый слой имеет положительный потенциал по отношению к основе, причем разность потенциалов увеличивается с увеличением числа рабочих ходов при ЭМО. Например, при обработке за два рабочих хода потенциал составляет 0 024 В, а при обработке за один рабочий ход - 0 018 В. Согласно теории больший положительный потенциал белой зоны обусловливает ее слабую травимость в стандартных растворах. [12]
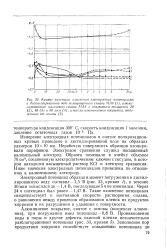
Измерения электродных потенциалов нестойкой азотированной зоны стали 25Х18Н8В2 после обработки в 10 % - ном растворе К2Сг2О7 при кипении и при 200Э ( в автоклаве) и измерения незащищенной поверхности показали, что защитная обработка приводит к некоторому облагораживанию поверхности слоя ( фиг. [13]
Измерение электродных потенциалов у микропар, имеющих крайне малые размеры, горизонтальное расположение и непосредственный контакт друг с другом, довольно затруднительно, однако обнаружить наличие работающей микропары на корродирующей поверхности можно, и для этого существуют специальные методы. [14]
Измерение электродных потенциалов в исследованных растворах проводилось обычным компенсационным методом по отношению к насыщенному каломельному электроду параллельно на четырех - пяти образцах в течение 7 - 9 час. [15]
Страницы: 1 2 3 4