Измерение - скорость - образование - пироуглерод
Cтраница 1
 |
Относительная скорость образования пироуглерода. [1] |
Измерения скорости образования пироуглерода на плоских пластинках платины и кварца при температурах 800 - 1000 С дали значения, мало отличающиеся от полученных для кварцевых нитей. Так, при 800 С константа скорости роста пироуглерода из метана на платине оказалась равной 4 2 - 10-и, тогда как на кварцевых нитях она имеет значение 4 5 - 10 11 г - см-2 сек 1 атм-1. [2]
В принципе измерение скорости образования пироуглерода в слое сажи заключается в следующем. Через обогреваемую снаружи реакционную трубку ( рис. 4.1) пропускают исследуемый углеводород или смесь углеводорода с водородом или инертным газом. Температура реакционной трубки и скорость потока газа поддерживаются постоянными. В реакционную трубку на определенное время вводят лодочку с навеской сажи, удельная поверхность которой известна. Взвешивание лодочки до и после опыта дает количество углерода, образовавшегося на поверхности сажи. [3]
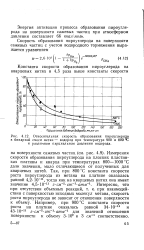
На рис. 4.9 даны результаты измерения скорости образования пироуглерода на саже и кварцевом волокне при 800 С. [4]
Методика описываемых опытов практически не отличалась от методики измерения скорости образования пироуглерода в слое сажи. [5]
Относительная скорость этих процессов может быть установлена только после измерения скорости образования пироуглерода из различных углеводородов, однако по этому вопросу имеется еще мало экспериментальных данных. Так, Окслей [8] указывает, что при 1000 С скорость образования пироуглерода из ацетилена в 182 раза выше, чем из метана, а при 1600 С эти скорости одинаковы. В работе [20] показано, что при температуре выше 1600 С скорости образования пироуглерода из метана и ацетилена практически одинаковы. По данным Брауна и Уотта ( см. табл. 4.9), скорости для бензола, метана и пропана при температурах 1600 - 2100 С отличаются менее чем на порядок. [6]
Методика измерения, по существу, не отличается от методики, применяемой для измерения скорости образования пироуглерода в слое сажи ( см. стр. Однако практически оказалось выгоднее измерять не абсолютную, а относительную скорость образования пироуглерода. Поэтому принципиально методика измерения заключается в том, что на определенное время в реакционную зону, в которой поддерживаются постоянные температура и скорость потока углеводорода, вводят две равные навески сажи: исследуемой и эталонной. [7]
 |
Схема установки для измерения скорости образования пироуглерода в слое сажи. [8] |
В результате первых измерений было показано, что реакция образования пироуглерода на поверхности имеет первый порядок по концентрации углеводорода. Для этого были проведены измерения скорости образования пироуглерода при различной концентрации углеводорода в смесях углеводород - азот при атмосферном давлении. [9]
Несмотря на большое число работ, процесс образования пироуглерода изучен недостаточно и надежных количественных данных о скорости образования пироуглерода пока очень мало. Это объясняется тем, что измерение скорости образования пироуглерода связано с большими трудностями. [10]
 |
Энергия активации и константа скорости процесса роста пироуглерода. [11] |
В связи с расширяющимся применением пироуглерода для ряда отраслей техники в последнее время опубликовано много работ, посвященных получению пироуглерода из различных углеводородов и изучению его физико-химических свойств. В большинстве случаев пироуглерод получается при относительно высоких температурах ( 1500 С), и результаты измерения скорости образования пироуглерода не свободны от диффузионного торможения и не могут быть использованы для надежного кинетического анализа. В связи с этим ниже приведены результаты лишь ряда типичных работ. [12]
 |
Относительная скорость образования пироуглерода из смесей метана, ацетилена и бензола с азотом при атмосферном давлении. т / - метан. 2 - ацетилен. 3 - бензол. [13] |
Из рис. 7 - 5 видно, что реакция образования пироуглерода имеет первый порядок по концентрации углеводорода. Такие значения получены при давлениях до 2 МПа. Измерение скорости образования пироуглерода при 1500 - 1900 С также показало, что реакция имеет первый порядок. Скорость образования углерода замедляется водородом, особенно при малых концентрациях. [14]
Страницы: 1