Измерение - теплота - растворение
Cтраница 3
Тепловыделением называют количество тепла в калориях на грамм негидратированного цемента, выделяющееся при его полной гидратации при определенной температуре. Наиболее распространенный способ определения тепловыделения заключается в измерении теплоты растворения негидратированного и гидратированного цемента в смеси азотной и фтористоводородной кислот: разница между этими двумя величинами представляет тепловыделение гидратации. [31]
Непрерывное термометрическое титрование было предложено для быстрого определения тепловых эффектов в системах, где протекает одна или несколько быстрых реакций. Хотя данный метод идеально приспособлен для определения теплот последовательных или одновременно протекающих реакций, он применим также и для однокомпонентных систем как быстрый и сравнительно точный способ измерения теплоты растворения, а также для получения обычных аналитических результатов. [32]
Полученное значение энтропии скорее всего относится к частной, несомненно неравновесной, конфигурации поверхности. Действительно ли экспериментальные поверхностные эффекты при измерении теплот растворения и теплюемкостей являются экстенсивными характеристиками, не зависящими от размера и формы кристаллов. Используя различные по размеру частиц фракции тонкодисперсного хлорида натрия, полученного методом испарения, Паттер-сон и др. [90] нашли, что вклад поверхности в низкотемпературную теплоемкость меняется приблизительно пропорционально удельной поверхности порошка, определенной по адсорбции газа. Такие же измерения было бы интересно провести и на образцах хлорида натрия, полученных другими методами. [33]
В предыдущих главах описан ряд методов оценки свободной, или полной, поверхностной энергии твердых тел. Обычно при использовании этих методов необходимо знать удельную поверхность исследуемого образца, определенную каким-нибудь независимым способом. Это относится, в частности, к методам измерения теплоты растворения ( см. гл. [34]
Такое сопоставление позволяет сделать вывод о несомненном влиянии аниона на температурную зависимость теплоты растворения. Интересно, что при растворении в воде, по-видимому, все сульфаты будут растворяться более экзотермично с повышением температуры. Примером могут служить приведенные в той же таблице результаты измерения теплот растворения CuS04 - 5H2O, ( NH4) 2S04, K2SO4 в воде при 25 и 45 С. [35]
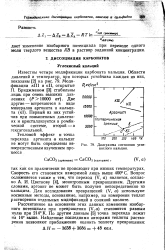 |
Диаграмма состояния углекислого кальция. [36] |
Скорость его становится измеримой лишь выше 400 С. Вопрос осложняется также и тем, что переход ( V, а) является, согласно А. И. Цветкову [4], монотропным превращением. Другими словами, аргонит не может быть получен непосредственно из кальцита. Для исследования превращений ( V, а) используют косвенные методы, основанные, например, на измерении теплот растворения отдельных модификаций в соляной кислоте. [37]
Страницы: 1 2 3