Измерение - упругость - пар
Cтраница 3
Весьма желательно выполнить ряд независимых исследований и подвергнуть критической проверке существующую методику измерений упругости паров. [31]
Здесь речь идет только о таких газах, чистоту которых нельзя доказать измерением упругости пара или точки плавления. Важным вспомогательным средством для идентификации газа являются также весы для определения плотности газа. [32]
Для определения молекулярного веса белков почти не применимы обычные методы, основанные на измерении упругости пара, повышения температуры кипения и понижения температуры замерзания растворов. [33]
Криоскопические измерения вследствие простоты эксперимента более распространены в практике физико-химического исследования, чем эбуллиоскопические или измерения упругости пара. [34]
Определение сегмента из термодинамических свойств разбавленных растворов полимеров, именуемого термодинамическим сегментом, может быть осуществлено измерением упругости пара растворителя над раствором полимера или измерением осмотического давления с использованием закона Рауля или закона Вант-Гоффа. [35]
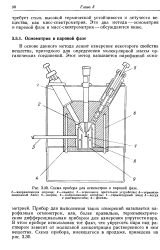 |
Схема прибора для осмометрии в паровой фазе. [36] |
Прибор для выполнения таких измерений называется па-рофазным осмометром, или, более правильно, термоэлектрическим дифференциальным прибором для измерения упругости пара. В этом приборе использован тот факт, что упругость пара над раствором зависит от моляльной концентрации растворенного в нем вещества. [37]
Данные основных исследований, выполненных методами термического [1, 9], микроструктурного [1, 6-9] и рентгеновского [1-8] анализов, а также измерениями упругости паров [1, 7] и определениями термодинамических свойств [1], как следует из приводимой ниже сводной табл. 318, несколько расходятся между собой. Основные расхождения сводятся к составу фаз, существующих в относительно узких областях составов: - 72 - 77 ( - 78 6 - 81 8 ат. Согласно диаграмме состояния системы Y - Zn, построенной в работе [1], в этих областях существуют химические соединения YZn4 и YZnn соответственно. Однако кристаллические структуры этих соединений в работе [1] идентифицированы не были. В работах [7, 8] было установлено, что в области составов - - 78 6 - 81 8 ат. В этой работе методом рентгеновского анализа исследовали сплавы, приготовленные в эквакуированных запаянных пирексовых трубках из иттрия и цинка чистотой 99 5 - 99 9 % и 99 99 % соответственно. Кристаллическая структура обоих соединений была идентифицирована и, кроме того, было убедительно показано, что аналогичные соединения с цинком существуют и для подавляющего большинства редкоземельных металлов аналогов иттрия. [38]
Высокие значения осмотического давления и вязкости более концентрированных растворов не позволяют применять к ним метод осмомет-рии, и в этих случаях необходимы измерения упругости пара. [39]
В то же время в данном случае нельзя использовать обычные методы определения величин активности ( электрохимические методы, методы, связанные с измерением упругости паров и пр. Экедал, Хог-фельдт и Силлен [23 ], рассматривая ионит как твердый раствор RMei и RMea, определили активности а и а2 и коэффициенты активности / i и / г для растворов различного состава. [40]
Если свободная слабая кислота или свободное слабое основание достаточно летучи, то можно определять их концентрацию или, точнее, их активность по измерению упругости пара. Практически истинную упругость пара не измеряют, а сравнивают летучесть вещества в растворе гидролизованной соли с летучестью ряда растворов с известными концентрациями. Так, например, в случае цианистоводородной соли щелочного металла свободная цианистоводородная кислота, получающаяся в результате гидролиза, обладает заметной летучестью. Ток воздуха пропускают с известной скоростью через раствор соли и с такой же скоростью - через раствор цианистого водорода. Концентрацию раствора цианистого водорода меняют до тех пор, пока его летучесть для данного раствора не станет такой же, как и летучесть в случае раствора соли. Можно считать, что концентрация или, вернее, активности свободной кислоты в обоих растворах одинаковы. [41]
Вследствие этого оба ряда наблюдений во многих случаях не могут быть между собой связаны и, в результате, обширный и весьма ценный материал, собранный при измерениях упругости пара, остается для теории неиспользованным. [42]
Как правило, соответствующее количество вещества, подлежащего исследованию ( в большинстве случаев 0 2 - 0 5 мл в жидком состоянии), помещают в трубку для измерения упругости пара, соединенную с точным ртутным манометром, внутренний диаметр которого должен быть не менее 8 мм; затем трубку, так же как и хорошо откачанный стандартный манометр, присоединяют к высоковакуумной аппаратуре. Лучше всего, если трубка заканчивается небольшим-тонкостенным шариком диаметром - 10 мм, чтобы жидкое или твердое вещество имело достаточно большую поверхность; часто применяют также узкие градуированные трубки, которые позволяют удобно установить приблизительное количество жидкости. Для измерения трубку вместе с газовым термометром ( тензиметрический термометр) помещают во вместительную, хорошо перемешиваемую ванну с охлаждающей смесью и производят отсчет показаний до тех пор, пока не получат совпадающих значений; легкое встряхивание вещества обеспечивает более быстрое установление равновесия. Для идентификации веществ или для оценки чистоты их фракций в большинстве случаев выбирают значения давления пара в области 20 - 200 мм рт. ст. Измерение более высоких упругостей пара осуществить уже труднее, так как для этого требуется особо хорошее постоянство температуры ( плавящаяся или кипящая жидкость для ванн); напротив, при небольших значениях упругости пара сильно сказываются понижение ртутного мениска и ошибки отсчета. [43]
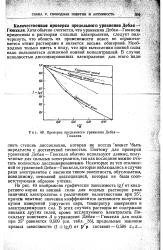 |
Проверка предельного уравнения Дебая - Гюккеля. [44] |
На рис. 49 изображена графически зависимость lg / от квадратного корня из ионной силы для водных растворов ряда типичных электролитов с различными валентностями при 25, причем опытные значения коэффициентов активности получены путем измерений упругости пара, температур замерзания и электродвижущих сил. [45]
Страницы: 1 2 3 4