Критическая изобара
Cтраница 1
Критическая изобара - изотерма является кривой третьей степени. Очевидно, что чем больше абсолютное значение третьей производной, тем уже область концентраций вблизи критической точки, в которой химический потенциал компонента мало зависит от состава раствора. [1]
Критическая изобара имеет в критической точке вертикальную касательную. Так как в остальных точках этой изобары выполняется неравенство ( ди / дТ) р0, то критическая точка одновременно является точкой перегиба. [2]
Критическая изобара горизонтально касается кривой насыщения в критической точке, которая является одновременно точкой перегиба. По мере удаления от критической точки перегиб изобар вырождается. [3]
Критическая изобара имеет в критической точке вертикальную касательную. Так как в остальных точках этой изобары выполняется неравенство ( ди / дТ) р0, то критическая точка одновременно является точкой перегиба. [4]
Критическая изобара горизонтально касается кривой насыщения в критической точке, которая является одновременно точкой перегиба. По мере удаления от критической точки перегиб изобар вырождается. [5]
Критическая изобара имеет в критической точке вертикальную касательную. Так как в остальных точках этой изобары выполняется неравенство ( dv / dT) p0, то критическая точка одновременно является точкой перегиба. [6]
Критическая изобара горизонтально касается кривой насыщения в критической точке, которая является одновременно точкой перегиба. По мере удаления от критической точки перегиб изобар вырождается. [7]
Ниже критической изобары картина существенно изменяется. Здесь левее кривой жидкости вещество находится в специфически жидком состоянии. В области, охватываемой пограничной кривой, сосуществуют жидкая и газообразная фазы, находящиеся в термодинамическом равновесии. Переход через область влажного насыщенного пара для вещества сопряжен с резким скачкообразным изменением его качественного состояния ( жидкость обращается в пар), причем разница в свойствах этих двух фаз весьма заметна именно потому, что они сосуществуют рядом. [8]
Проведя критическую изобару ркр, можно в диаграмме различить следующие области: правее верхней пограничной кривой и отрезка изобары ркр - область перегретого пара; внутри пограничной кривой - область влажного пара; левее изобары ркр - область сверхкритического давления, подробно рассмотренная при изучении ри-диаграммы водяного пара. [9]
Изучение формы критических изобар - изотерм v - Л; и h - NI вблизи критической кривой открывает возможность исследовать влияние особенностей системы с азеотропизмом в критической области на объемное и термодинамическое поведение этих систем в закритиче-ской области. [10]
Для изобар выше критической изобары связь должна получаться или со значениями 5 ( причем последние должны быть известны вдоль какой-либо изотермы выше критической температуры), или от принятия в уравнении ( 18) за нижний предел Т0 температуру ниже критической и от приведения, на основании известных удельных объемов жидкости, энтропии к энтропии насыщенной жидкости. [11]
 |
Теплоемкости и показатель.| Изобары реального газа в V, / - диаграмме.| Изохоры реального газа в р, / - диаграмме. [12] |
При давлениях выше критических изобары теплоемкости с имеют вид кривых с максимумом, причем максимумы тем выше и острее, чем ближе данная изобара к критической. Наличие этих максимумов в надкритической области означает, что при изобарном переходе ( при р ркр) из жидкости в пар необходимо затратить дополнительную энергию, преодолеть тепловой барьер, являющийся аналогом теплоты парообразования г при докрити-ческом переходе. В этом заключается одна из основных особенностей надкритического состояния. [13]
Линия, соответствующая критической изобаре, располагается на диаграмме наиболее круто. Отсюда и следует, что критическая точка К, разделяющая пограничные кривые х 0 и х 1, лежит на левом склоне криволинейного треугольника, а не на вершине его, как в р - v и Т - S координатах. [14]
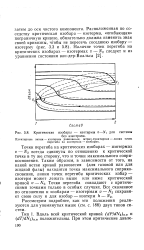 |
Критические изобары - изотермы v - NJ для системы. [15] |
Страницы: 1 2 3 4