Изогексан
Cтраница 1
Изогексан разделяется в 30-тарелочной колонне диаметром 1 83 ж и высотой 27 5 м при давлении 2 1 am, температура верха колонны 46 С. [1]
Изогексан имеет в целом шесть атомов углерода, а изогексиль-ная группа образуется при отнятии одного атома водорода от С-атома, находящегося на конце, противоположном разветвлению. [2]
Первый изогексан называется 2-метилпентаном, а второй 3-метилпентаном. [3]
Образующиеся изогексаны могут претерпевать дальнейшие превращения - расщепление и изомеризацию. В обычных условиях гидрокрекинга бензольное кольцо, как правило, не гидрируется или гидрируется в очень незначительной степени; при введении в бензольное кольцо метильных заместителей гидрирование облегчается. Повышение температуры гидрокрекинга способствует превращению бензольного кольца в изопарафиновые углеводороды. [4]
 |
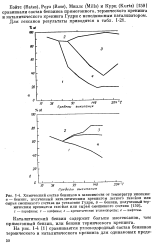
Влияние давления на выход продуктов реакции при каталитическом риформинге бензиновой фракции 62 - 105 С. [5] |
Отношения изогексаны: н-гексан и изогептаны: н-гептан возрастают по мере уменьшения объемной скорости подачи сырья. [6]
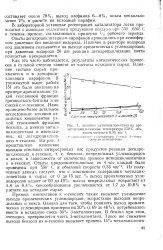 |
Влияние етилциклопелтана на ароматизацию н-гексана. температура 550 С, объемная скорость 0 35 час 1. [7] |
Примесь изогексанов к н-гексану также вызывает уменьшение выхода ароматических углеводородов, возрастание выходов непредельных и кокса. Однако для того, чтобы понизить выход ароматических углеводородов примерно на 20 % ( с 69 до 46 %), потребовалось ввести в исходную смесь 50 % 3-метилпентана. В бензол при этом, очевидно, превращается часть 3-метилпентана. [8]
Изопентан и изогексаны могут быть получены методом каталитической изомеризации. Подвергая легкий прямогонный бензин изомеризации, можно значительно повысить его октановое число. [9]
Изопентан, изогексан и изогептан присутствовали в больших количествах, чем соответствующие нормальные парафины. [10]
Фотохимическое окисление изогексана ( 2-метилпен-тана) дает гидроперекись, образованию которой способствует присутствие инициатора - перекиси бензоила. [11]
В катализатах изогексанов не наблюдается такого резкого количественного различия между углеводородами с двойной связью у первого углеродного атома и углеводородами с двойной связью ближе к центру углеродной цепочки. [12]
В отличие от изогексанов и изогексенов строение н-гексана допускает образование не только пяти -, но и шестичленного цикла. Поэтому, проследив зависимость скоростей обоих видов дегидроциклизации от состава исходной реакционной смеси, в частности от присутствия в ней олефина, можно было судить о сходстве или различии реакций Св - и С3 - дегидроциклиза-ции алканов. [13]
Зная, что гидроперекись изогексана при нагревании с 2-ме-тилпропаном дает диметилпропилкарбинол, предложите механизм разложения этой гидроперекиси. [14]
Страницы: 1 2 3 4