Низкоосновные аниониты
Cтраница 1
Низкоосновные аниониты, полученные сополимеризацией 2-метил - 5-ви-нилпиридина с диэфирами этиленгликоля, полиэтиленгликолей и мета-криловой кислоты, являются вполне подходящими для очистки сточных вод от фенолов. [1]
Низкоосновные аниониты, содержащие основные группь - NH2, NH, N. [2]
Для получения аминокарбоксильных амфолитов используют низкоосновные аниониты, полученные путем поликонденсации полиэтиленполиаминов с формальдегидом и эпихлоргидрином или олигомеров последнего с аммиаком и аминами. [3]
Исходя из указанных предпосылок, авторы синтезировали низкоосновные аниониты - Исевиты АНС-2-15, АНС-2-24, АНС-3, способные разделять молибден и вольфрам. [4]
Анионит представляет собой твердый, нерастворимый в воде материал, способный вступать в реакцию ионного обмена с кислотами. Различают низкоосновные аниониты, вступающие в реакцию с сильными кислотами, и высокоосновные катиониты, вступающие в реакцию с кремниевой кислотой. Образующиеся в рез утате этих реакций соответственно СО2 и Н2О остаются в обессоливаемой воде, а остальные соединения остаются в фильтрующем материале. По мере работы фильтры теряют исходную обменную способность и для ее восстановления их регенерируют, промывая соответствующими растворами. [5]
Синтезированы иониты специально для работы в газовых средах. Показано, что низкоосновные аниониты по своим сорбцион-ным свойствам относительно углекислого газа превосходят минеральные поглотители и могут поглощать СОо как из сухого, так и из влажного воздуха. [6]
Сиротермиониты пока не находят широкого применения в практике ввиду сложности получения ионитов регулярной структуры, обладающих высокой степенью гидролиза. К тому же слабокислотные катиониты и низкоосновные аниониты обладают большой селективностью к ионам переходных металлов и вряд ли могут быть регенерированы только в термоводной среде без применения химических реагентов, поскольку в процессе эксплуатации в ионите будут накапливаться ионы переходных металлов. [7]
Так, например, в соответствии с общими свойствами комплексных соединений в растворах, селективны к урану и железу катиониты с кислородсодержащими ( карбоксильными, фосфорнокислыми) функциональными группами. По аналогичным причинам к металлам, находящимся в середине четвертого периода периодической системы Д. И. Менделеева, селективны низкоосновные аниониты. [8]
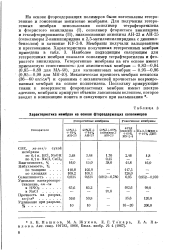 |
Характеристика мембран на основе фторсодержащих сополимеров. [9] |
На основе фторсодержащих полимеров были изготовлены гетерогенные и гомогенные ионитовые мембраны. Для получения гетерогенных мембран использовали сополимер тетрафторэтилена и фтористого винилидена ( I), сополимер фтористого винилидена и гексафторпропилена ( II), низкоосновные аниониты АН-23 и АН-25 ( сополимеры 2-винилпиридина и 2 5-метилвинилпиридина с дивинил-бензолом) и катионит КУ-2-8. Мембраны получали вальцеванием и прессованием. Наиболее подходящим связующим для гетерогенных мембран оказался сополимер тетрафторэтилена и фтористого винилидена. Механическая прочность мембран невысока ( 36 - 60 кгс / см2) и сравнима с механической прочностью неармированных мембран на основе полиэтилена. [10]
 |
Схематичное изображение гелевидной ( а и макропористой ( б ионообменных смол. [11] |
Сополимеризацией виниловых мономеров, содержащих кислотные группы, получают разнообразные катиониты, нек-рые из к-рых выпускают в промышленном масштабе. Слабокислотные катиониты получают, напр. Низкоосновные аниониты синтезируют сополимеризацией аллиламинов, винилпиридинов, аминостирола с дивинилбензолом или др. дивинильными соединениями. [12]
В ходе исследований показано, что значительное влияние на сорбционное поведение ионов металлов оказывает характер фонового электролита. В нитратных и сульфатных электролитах, обладающих низкой комплексообразующей способностью, сопутствующие металлы в основном присутствуют в виде положительно заряженных ионов. Поэтому, в основном, они поглощаются сорбентами, имеющими катионообменные группы. В этих средах аниониты практически не сорбируют ионы тяжелых цветных металлов, ионы железа, кальция, магния. В отсутствие в растворах сильного комплек-сообразователя платиноиды находятся в виде непрочных комплексов с анионами или молекулами воды. В этом случае они поглощаются высокоосновными анионитами в виде нейтральных комплексных соединений, о чем свидетельствует максимум на зависимости сорбируемости металла от концентрации соответствующей кислоты. Низкоосновные аниониты, содержащие в структуре функциональных групп атомы азота с неподеленной парой электронов, поглощают платиноиды еще и за счет комплексообразо-вания. Установлено, что сорбируемость увеличивается с повышением прочности связи металл - ионогенная группировка в следующем ряду: монодентатные низкоосновные аниониты монофункциональные пиридиновые аниониты, бидентатные низкоосновные аниониты хелатные пиридиновые аниониты, аминокарбоксильные и аминофос-форнокислые амфолиты амфолиты на основе винилпиридина. Кроме того, аминокарбоксильные и фосфорнокислые амфолиты из указанных растворов в некоторой степени поглощают ионы тяжелых цветных металлов за счет образования хелатных комплексов. [13]
В ходе исследований показано, что значительное влияние на сорбционное поведение ионов металлов оказывает характер фонового электролита. В нитратных и сульфатных электролитах, обладающих низкой комплексообразующей способностью, сопутствующие металлы в основном присутствуют в виде положительно заряженных ионов. Поэтому, в основном, они поглощаются сорбентами, имеющими катионообменные группы. В этих средах аниониты практически не сорбируют ионы тяжелых цветных металлов, ионы железа, кальция, магния. В отсутствие в растворах сильного комплек-сообразователя платиноиды находятся в виде непрочных комплексов с анионами или молекулами воды. В этом случае они поглощаются высокоосновными анионитами в виде нейтральных комплексных соединений, о чем свидетельствует максимум на зависимости сорбируемости металла от концентрации соответствующей кислоты. Низкоосновные аниониты, содержащие в структуре функциональных групп атомы азота с неподеленной парой электронов, поглощают платиноиды еще и за счет комплексообразо-вания. Установлено, что сорбируемость увеличивается с повышением прочности связи металл - ионогенная группировка в следующем ряду: монодентатные низкоосновные аниониты монофункциональные пиридиновые аниониты, бидентатные низкоосновные аниониты хелатные пиридиновые аниониты, аминокарбоксильные и аминофос-форнокислые амфолиты амфолиты на основе винилпиридина. Кроме того, аминокарбоксильные и фосфорнокислые амфолиты из указанных растворов в некоторой степени поглощают ионы тяжелых цветных металлов за счет образования хелатных комплексов. [14]
В ходе исследований показано, что значительное влияние на сорбционное поведение ионов металлов оказывает характер фонового электролита. В нитратных и сульфатных электролитах, обладающих низкой комплексообразующей способностью, сопутствующие металлы в основном присутствуют в виде положительно заряженных ионов. Поэтому, в основном, они поглощаются сорбентами, имеющими катионообменные группы. В этих средах аниониты практически не сорбируют ионы тяжелых цветных металлов, ионы железа, кальция, магния. В отсутствие в растворах сильного комплек-сообразователя платиноиды находятся в виде непрочных комплексов с анионами или молекулами воды. В этом случае они поглощаются высокоосновными анионитами в виде нейтральных комплексных соединений, о чем свидетельствует максимум на зависимости сорбируемости металла от концентрации соответствующей кислоты. Низкоосновные аниониты, содержащие в структуре функциональных групп атомы азота с неподеленной парой электронов, поглощают платиноиды еще и за счет комплексообразо-вания. Установлено, что сорбируемость увеличивается с повышением прочности связи металл - ионогенная группировка в следующем ряду: монодентатные низкоосновные аниониты монофункциональные пиридиновые аниониты, бидентатные низкоосновные аниониты хелатные пиридиновые аниониты, аминокарбоксильные и аминофос-форнокислые амфолиты амфолиты на основе винилпиридина. Кроме того, аминокарбоксильные и фосфорнокислые амфолиты из указанных растворов в некоторой степени поглощают ионы тяжелых цветных металлов за счет образования хелатных комплексов. [15]
Страницы: 1