Изопропь
Cтраница 1
Изопропи ] 0) 5ый спирт нашел применение как растворитель, п ( многих случаях заменяющий этиловый спирт; для масел, жирсм и смол изопропилоный спирт является даже лучшим растаорите лем, чем этилопт гй. [1]
Получение изопропи л - 1 - ц иклобутанон а-2 Степень ненасыщенности изопропилиден-1 - циклобутанона-2 определяется присоединением водорода в присутствии платиновой черни; давление водорода близко к атмосферному; температура комнатная. [2]
Чаще всего встречающиеся вторичные спирты, а именно: изопропи - - ловый, erop - бутиловый и пентанол-2, в отсутствие этилового спирта, ме-тилкетонов и эфиров молочной кислоты, можно обнаружить по реакции образования йодоформа56, так как они содержат группу СН3СНОН -, связанную с атомом углерода. Однако в некоторых смесях растворителей образование йодоформа трудно обнаружить. [3]
В качестве растворителей нефтерастворимого деэмульгатора тримепяются низкомолекулярные спирты ( метиловый, изопропи - ловый и др.), ароматические углеводороды и их смеси в различных соотношениях. [4]
Все изученные изопропилбензолы участвуют в реакции ионного гидрирования и располагаются в ряд: поли - л-изопропил стирол изопропи л бензол 1 4-метилизопропилбензол - 1 3 5-триизопропилбензол. [5]
Для окисления спирта по Оппенауэру к его раствору в сухом бс золе прибавляют / npem - бутилат алюминия и избыток ацетона; i следний восстанавливается до изопропи левого спирта; спирт j взятый в реакцию, окисляется. [6]
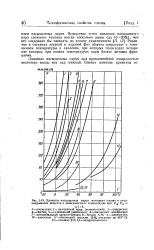 |
Давление насыщенных паров моторных топлйв и индивидуальных веществ в зависимости от температуры при Кж. Кп. [7] |
Б-70; 9-авиабеняин; 10-изооктан; / / - бакинский керосин ( 30 % выкипает до 200 С); 12 - топливо T-I; 13 - изопропи. [8]
Этот радикал не способен к распаду на олефин и атом брома, и единственно возможные пути его реакций - это рекомбинации с другим таким же радикалом или с атомом брома. Таким образом, в случае изопропи л бромида цепь не может развиваться, и реакция происходит лишь путем простого мономолекулярного распада с энергией активации 47 ккал. Это приводит к тому, что суммарная энергия активации цепного процесса ( 40 - 42 ккал) оказывается примерно на 10 ккал ниже энергии активации ( 50 7 ккал) простого мономолекулярного распада. [9]
CeHia 1) C7Hl4, J С8 нц C Hi8 CioH2o CiiH2a Cl2H84 CisH26 Ci4H28 Ci5H o CieH82 1 -цис - 3 - Днметилциклогек-сан 1 -транс - 3 - Димети лцикло-гексан 1 -цис - 4 - Диметилшп логек-сан 1 -транс - 4 - Димети лцикло-гексан н - Пропилциклогексан Изопропилциклогексан 1, 1 3 - Триметилциклогексан н - Бу ти лцик логексан Изобутилциклогенсан втор. Бутилциклогексан 1 - Мети л-цис-4 - изопропи л-циклогексан ( - Метил-транс - 4-изопро-пилциклогексан 2 - Цяклогексил-2 - метилбу-тан ( трет. [10]
Отделение хлористого калия способствует протеканию реакции. Применение бромистых и йодистых солей менее удобно, так как КВг и KI растворимы в изопропи. [11]
Гофман проводил разложение амидов кислот таким образом, что растворял амид в эквимолекулярном количестве брома и затем добавлял калийную щелочь. Так приготовил он м е т и л - и э т и л-амины с выходами в 87 соответственно 80 - 90 %, далее-про-пила мин ( 80 - 90 %), изопропи л ам ин ( 60 - 70 %), изобу-ти л а м ин ( 90 %), амиламин ( 88 %), изоамиламин ( 88 %), гексиламин ( ок. Октнл-амин и иониламин получались с очень плохими выходами, так как здесь сильно преобладало образование нитрилов. [12]
Хотя для реакции восстановления были испробованы, различные металлы в виде их алкоголятов, в том числе этилат магния [2], хлормагнийэтилат [2], иод - и броммагний алкоголяты [11], а также алкоголяты натрия [1], олова и-циркония [12], однако до сего времени наилучшими реагентами для этой цели считаются алюминиевые производные. Их преимущества заключаются в том, что они обладают гораздо более мягким конденсирующим действием, чем алкоголяты натрия или магния, и растворимы как в спиртах, так и в углеводородах. Превосходство изопропи - - лата алюминия по сравнению с этилатом алюминия заключается в том [1,3] что ПРИ применении изоттропилата реакция, как правило, идет быстрее, побочные реакции5 протекают в меньшей степени и выход продукта реакция; увеличивается. [13]
Трехгорлый 4-литровый металлический сосуд снабжают мешалкой, трубкой для ввода газа и стеклянной отводной трубкой длиной 60 см, защищенной осушительной трубкой. Сосуд продувают азотом и суспензию катализатора готовят следующим обрачон: 2 л цнклогексана помещают в реактор, затем добавляют 200 мл 0 2 М раствора тетрадецнллитийалюминия, приготовленного по ранее описанной методике. Смесь охлаждают в водяной бане и добавляют 0 029 моля четыреххлорнстого титана в виде раствора в циклогексане. Смесь сразу же приобретает черно-коричневую окраску и с этого момента является активным катализатором для полимеризации этилена. Баллон с этиленом присоединяют к вводной трубке через предохранительную ловушку. Этилен барботируют через интенсивно перемешиваемую суспензию катализатора; начинается выпадение полиэтилена с выделением некоторого количества тепла. Полимеризацию можно продолжать сколько угодно долго, практически до тех пор, пока еще возможно перемешивание раствора. Смесь полимера и растворителя, содержащего катализатор, выливают в большой избыток изопропи. Продукт обычно получают в виде белого порошка, из которого можно отлить прозрачные упругие пленки или вытянуть упругие нити. [14]
Страницы: 1