Изотерма - адсорбция - пар - азот
Cтраница 1
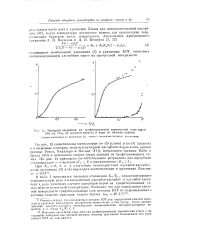 |
Изотермы адсорбции на графитированпой термической саже паров. [1] |
Изотерма адсорбции пара азота на графитированных термических сажах с однородной поверхностью вначале вогнута, поэтому при малых заполнениях она уравнением БЭТ не описывается. [2]
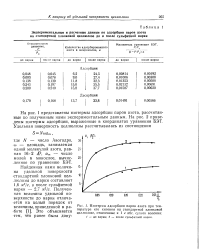 |
Изотермы адсорбции паров азота при температуре его кипения на стандартной хлопковой целлюлозе, отнесенные к 1 г абс. сухого волокна. [3] |
На рис. 1 представлены изотермы адсорбции паров азота, рассчитанные по полученным нами экспериментальным данным. На рис. 2 приведены изотермы адсорбции, выраженные в координатах уравнения БЭТ. [4]
 |
Изобаты адсорбции гексана на синтетическом цеолите СаА в линейной форме по уравнению ( 7. [5] |
Исходной для вычислений служила изотерма адсорбции паров азота на шабазите при - 183 [18], по которой были найдены константы W0 и В для азота как стандартного пара. [6]
Влияние дегидратации поверхности кремнезема на изотермы адсорбции паров азота и аргона. [7]
На рис. 13 сопоставлены вычисленные по ( 3) ( слева) и по ( 4) ( справа) и измеренные изотермы нолимолекулярной адсорбции паров азота, аргона ( данные Росса, Уинклера и Пальца 17 ]), метиламина ( данные Биби и Делла 133 ]) и метилового спирта ( наши данные) на графитированных са-жах. [8]
При рассмотрении данных табл. 29 обращает на себя внимание тот факт, что величины внутренней поверхности волокон, вычисленные по изотермам адсорбции паров СН3ОН, СаН5ОН и СН3СООН, в несколько раз больше, чем по изотермам адсорбции паров азота. Это может свидетельствовать о том, что процесс сорбции этих паров сопровождается набуханием целлюлозных волокон; степень набухания волокон различна в зависимости от размера, строения молекул и их способности к донорно-акцепторным взаимодействиям с гидроксильными группами целлюлозы и нарушению водородных связей в структуре целлюлозы. [9]
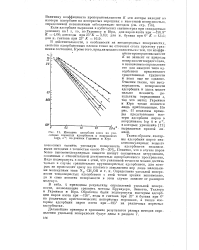 |
Изотерма адсорбции азота на различных пористых адсорбентах в координатах log /., а-2, по данным Гаркинса и Юра. [10] |
В табл. 4 приведены результаты определений удельной поверхности, позволяющие сравнить методы Брунауера, Эмметта, Теллера и Гаркинса и Юра. Обработке были подвергнуты изотермы адсорбции паров азота при - 195, воды и гептана при 25 и бутана при 0 на различных кристаллических непористых порошках, а также изотермы адсорбции паров азота при - 195 на различных пористых адсорбентах. [11]
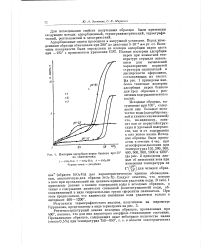 |
Изотермы адсорбции паров бензола при 20 на силикагелях. [12] |
Перед измерениями образцы откачивали при 280 до давления 3 - 10 6 мм рт. ст. Величины поверхности были определены из изотерм адсорбции паров азота при - 195 с применением уравнения БЭТ. [13]
В табл. 4 приведены результаты определений удельной поверхности, позволяющие сравнить методы Брунауера, Эмметта, Теллера и Гаркинса и Юра. Обработке были подвергнуты изотермы адсорбции паров азота при - 195, воды и гептана при 25 и бутана при 0 на различных кристаллических непористых порошках, а также изотермы адсорбции паров азота при - 195 на различных пористых адсорбентах. [14]
С этим связан недостаток их метода определения-поверхности, так как допущение о начале капиллярной конденсации, происходящем обязательно на поверхности мономолекулярного слоя, игнорирует возможную полимолекулярную адсорбцию паров, а подчинение первоначального адсорбционного процесса вплоть до образования конденсированного слоя уравнению Лэнгмюра не отвечает действительности. Сравнительное применение методов Брунауера, Эмметта и Теллера и Гаркинса и Юра, с одной стороны, и методов Кистлера, Фишера и Фримена и Гарвея, с другой стороны, сделанное Джойнером, Вейнбергером и Монтгомери48, к изотермам адсорбции паров азота и бутана на различных адсорбентах показало, что величины s, получаемые по методам капиллярной конденсации, значительно превышают величины s, определяемые двумя первыми методами, которые давали близкие результаты. [15]
Страницы: 1 2