Пептидной антибиотик
Cтраница 1
Большинство пептидных антибиотиков имеет циклическую структуру, которая может содержать помимо пептидной сложноэфирную и другие виды химических связей. Циклическое строение, а также наличие в молекуле D-аминокислот и других небелковых элементов придает таким антибиотикам высокую устойчивость к протеолитическим ферментам. Часто сложная структура препятствует широкому использованию химического синтеза. Из-за высокой токсичности систематическое применение находят лишь отдельные пептидные антибиотики. [1]
Биосинтез пептидных антибиотиков осуществляется по принципу, отличному от принципа биосинтеза белков на рибосоме. [2]
В группе пептидных антибиотиков наблюдается значительное структурное различие, тем не менее появляется все больше доводов в пользу того, что пептидные связи здесь создаются подобно тому, как это происходит при синтезе грамицидина. Поэтому результаты приведенных выше работ имеют как теоретическое, так и прикладное значение для производства других пептидных антибиотиков. [3]
С-Фенилглицин содержится в некоторых гетеромерных ге-теродетных циклических пептидных антибиотиках, например в остреогрицине и факторе S стафиломицина. [4]
Этот тип связей преобладает в различных пептидных антибиотиках ( разд. [5]
Третий, достаточно общий структурный фактор пептидных антибиотиков - это вид полипептидной ( или депсипеп-тидной) цепочки: либо это открытая классическая цепь, либо циклополи-пептидная структура, либо комбинированная система из цикла и открытой цепочки, либо система нескольких небольших циклов. [6]
Далее будут рассмотрены подробнее некоторые представители пептидных антибиотиков, причем для их классификации использовали рекомендации Хассаля [797], основывающиеся на механизме действия антибиотика. [7]
Аминомасляная кислота и фенилглицин обнаружены в пептидных антибиотиках лишь несколько лет назад. Известно очень ограниченное число пептидов, содержащих эти аминокислоты. [8]
Метод масс-спектрометрии особенно удобен при выяснении структуры пептидных антибиотиков, присутствие в которых непротеиногенных аминокислот и о-энантиомеров исключает использование ферментативного расщепления. [9]
Важное место занимают и исследования по химии пептидных антибиотиков. [10]
 |
Предполагаемая сандвичевая структура одного из аналогов валииомицииа. [11] |
Промежуточное положение между ионофорами и второй группой мем-браноактивных пептидных антибиотиков занимает аламетицин. Аламети-Цин вместе с природными аналогами сузукациллином и трихотоксином причисляют к амфифильным пептидным антибиотикам, которые в липид - Hbix мембранах создают флуктуирующий, независимый от напряжения поток ионов и поэтому представляют большой интерес как модельные системы нервной проводимости. [12]
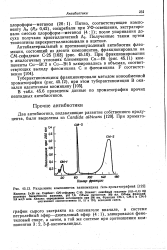 |
Разделение компонентов ванкомицина гель-хроматографией. [13] |
В табл. 45.6 приведены данные по хроматографии прочих пептидных антибиотиков. [14]
Как и в случае пенициллинов, для большинства пептидных антибиотиков существуют группы индивидуальных вещзств, которые удается различать с поиощыо хроматографии на бумаге. К таким группам относятся полимнксины ( включая аэроспорин и циркулин), бацитрацины, грамицидины и тироцидины, лихениформины, актиномицины, геомицины, латероснорины, иисины, стрептолины, эннаатины. [15]
Страницы: 1 2 3