Вычисление - константа - устойчивость
Cтраница 1
Вычисление констант устойчивости в системах, в которых происходит конкурентное комплексообразование, сильно упрощается, если имеются только комплексы состава 1: 1, например при амирюполикарбоксилат-ных или полиаминовых лигандах. Кроме того, эти комплексы настолько стабильны, что можно пренебречь свободными концентрациями тех из веществ М, М, L или L, избытка которых не имеется. [1]
Вычисление констант устойчивости комплексных соединений и констант протолитической диссоциации графически по точкам пересечения продолжений линейных участков или вычисление этих величин с помощью вспомогательных функций. [2]
Рассмотренные методы вычисления констант устойчивости применены при исследовании комплексообразующей способности многих соединений. Ниже приведены примеры вычисления констант устойчивости и состава комплексов на основании данных полярографического анализа. [3]
Уравнение ( 11 - 10) также использовалось в вычислениях констант устойчивости для систем, в которых образуется один или несколько катионных комплексов, но распределяется только свободная центральная группа. Предположение, что 1 пренебрежимо мало по сравнению с еР0, возможно, оправданно также для системы сульфата железа ( III) [62], поскольку заряд на В равен трем, в то время как ВА - только однозарядный. [4]
Так как потенциалы элементов ( 7 - 15), ( 7 - 15а) и ( 7 - 17) являются функциями двух концентрационных переменных, то вычисление констант устойчивости из измерений Е ( В, А) и Е ( В, А, Н) более сложно, чем для элементов только с одной переменной концентрацией. [5]
Измерения концентрации водородных ионов можно также провести для изучения комплексообразования в целом ряде систем В, А, Н, где лиганд А способен соединяться с протонами; применимость этого метода и вычисление констант устойчивости из экспериментальной функции h ( B, A, H) рассматриваются в разд. [6]
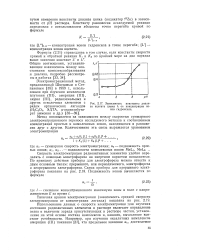 |
Зависимость константы диализа ацетата цинка К от концентрации ионов гидроксила. [7] |
Использование данных о скорости электромиграции для изучения состояния радиоактивных элементов в растворе включает определение знака и величины заряда присутствующих в растворе частиц, установление на этой основе состава комплексов и, наконец, вычисление констант устойчивости. [8]
При исследовании и применении комплексных соединений в анализе могут возникнуть следующие задачи: 1) установление природы и количества комплексных частиц в растворе; 2) определение состава комплексов в растворе; 3) вычисление констант устойчивости по известным концентрациям комплексных ионов; 4) определение молярных долей металла или лиганда, связанных в комплекс, а также отдельных комплексных частиц. [9]
Вычисление констант устойчивости комплексов высокой прочности ( рК 10) по кривым титрования основанием смеси комплексона и катиона не всегда дает положительные результаты. [10]
Вычисление констант устойчивости комплексов высокой прочности ( рК 10) по кривым титрования основанием смеси комплексона и катиона не всегда дает положительные результаты. [11]
Рассмотренные методы вычисления констант устойчивости применены при исследовании комплексообразующей способности многих соединений. Ниже приведены примеры вычисления констант устойчивости и состава комплексов на основании данных полярографического анализа. [12]
Среднее число лигандов, приходящееся на ион металла в фазе ионита, п равно отношению [ Хь ] / См и связано с константами устойчивости р обычными соотношениями. Единственная трудность, возникающая при вычислении констант устойчивости по результатам рН - метрического титрования, связана с отсутствием данных о концентрации ионов водорода в фазе ионита. [13]
Как бы то ни было, авторы полагают, что исследователи, имеющие дело с определением констант устойчивости, уделяют недостаточное внимание методам, используемым в других областях. Так, при конструировании оптических линз в течение нескольких лет успешно применялся алгоритм, основанный на методе ослабленных наименьших квадратов [44 - 47, 60, 61] Марквардта. Проблемы в этой области имеют много общего с вычислением констант устойчивости, поскольку и в том, и в другом случае существует большое число подлежащих оценке параметров, которые могут быть в различной степени коррелированы. Оказалось, что методы Марквардта и Флетчера - Пауэл-ла наиболее доступны, причем первый даже несколько предпочтительнее благодаря его успешному практическому применению. Это особенно справедливо для случая, когда ослабляющий множитель неизвестен и определяется не эмпирически, а специально рассчитывается для каждой итерации [66] или для каждого параметра на каждой итерации. [14]
Кинетические методы имеют ограниченное применение и их используют преимущественно при исследовании инертных комплексов. В равновесных методах определяют концентрации участников реакции, которые для инертных комплексов могут быть найдены путем химического анализа, а в случае лабильных комплексов их находят с помощью различных физико-химических методов. Общепринятая процедура заключается в определении всех или некоторых равновесных концентраций комплексообразователя, лиганда или комплексных соединений и часто включает нахождение вторичных концентрационных переменных, а затем вычисление констант устойчивости и химического сродства ДС реакции образования комплекса. [15]
Страницы: 1 2