Активирование - аминокислота
Cтраница 1
Активирование аминокислот на первом этапе биосинтеза приводит к тому, что молекулы их становятся гораздо более активными, более реакционноспособны-ми, что облегчает взаимодействие их друг с другом. В лабораторных условиях, для того чтобы соединить аминокислоты друг с другом, химик должен предварительно активировать их по линии либо карбоксильной, либо аминной группы введением какого-нибудь радикала. Только после этого аминокислоты могут взаимодействовать друг с другом. В организме активация аминокислот происходит иными, более мягкими путями, чем это обычно делает химик. В некоторой степени это вещество нам уже известно, так как это один из обычных нуклеотидов - адениловая кислота ( см. стр. [1]
Активирование аминокислот происходит в жидкой, неструктурной части цитоплазмы при участии соответствующих ферментов. [2]
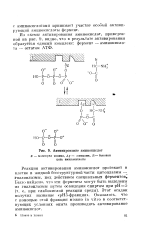 |
Активирование аминокислот. [3] |
Из схемы активирования аминокислот, приведенной на рис. 9, видно, что в результате активирования образуется единый комплекс: фермент - аминокислота - остаток АТФ. [4]
Вслед за активированием аминокислоты наступает второй этап ( см. рис. 8), когда в ход процесса включается РНК, притом определенная и своеобразная ее фракция. Это так называемая растворимая РНК, которая содержится в гиалоплазме и отличается от других высокополимерных фракций РНК, содержащихся в клеточных органоидах. [5]
Такой прием часто назы - ( аают активированием аминокислоты. [6]
В отличие от синтеза пептидов, при активировании аминокислот образуется не ацилфосфат и АДФ, а комплексное соединение аминокислоты с адениловой кислотой ( так называемый аденилат аминокислоты) и выделяется неорганический пиро-фосфат. [7]
 |
Примерная форма рибосомы, димера и субъединиц, образующихся при изменении кон. [8] |
Синтез белков из аминокислот происходит в четыре стадии: активирование аминокислот; соединение аминокислот с рибонуклеиновой кислотой; образование пептидной связи; освобождение синтезированной молекулы белка от рибосомы. [9]
Из результатов этих исследований сделан вывод о наличии процесса активирования аминокислот, при котором образуются соединения аминоацилов с адениловой кислотой, связанные с ферментом. Эти данные показали также, что для каждой из изученных аминокислот имеется отдельный фермент или участок фермента. [10]
Наиболее надежные результаты получены Замечником, Липманом и другими исследователями, учитывавшими первые стадии активирования аминокислот и их прикрепление к РРНК и стремившимися упростить систему, исследуя последнюю постадийно, а не брать ее во всей сложности. [11]
Соединение, возникающее в этой реакции, называется ацил-аденилатом аминокислоты, а самая реакция называется реакцией активирования аминокислот. Каждая из 20 аминокислот имеет свой специфический фермент, катализирующий эту реакцию. Подобные ферменты найдены во всех клетках и тканях, где их искали, - в бактериях и простейших, в тканях растений и высших животных, - словом, повсюду. Даже химически столь близкие аминокислоты, как валин и лейцин, требуют различных специфических ферментов для активирования. [12]
Белковый синтез, или процесс трансляции, может быть условно разделен на 5 стадий, из которых две считаются подготовительными и завершающимися, в частности активирование аминокислот и постсинтетическая модификация белковой молекулы, и 3 стадии составляют собственно трансляцию. [13]
Считается, что в молекуле каждой аминоацил-т РНК-синтетазы имеется по крайней мере 3 центра связывания: для аминокислоты, тРНК и АТФ; ферменты весьма чувствительны также к аналогам аминокислот, которые ингибируют активирование соответствующих аминокислот. Некоторые ферменты состоят из одной полипептидной цепи, другие-из двух или четырех гомологичных или гетерогенных субъединиц. [14]
 |
Этапы синтеза белка. [15] |
Страницы: 1 2