Окислительная активность
Cтраница 2
Окислительная активность элементов этой группы выражена сильнее, чем элементов V группы главной подгруппы: они непосредственно взаимодействуют со многими металлами и неметаллами. [16]
Окислительная активность вещества, содержащего элемент-окислитель, возрастает с уменьшением прочности связей в его молекулах. Это связано с одновременным повышением прочности кислот благодаря уменьшению числа несвязывагощих и увеличению числа связывающих электронных пар в их молекулах. Если соединение образовано элементом в очень устойчивой степени окисления, то непрочность соединения не делает его окислителем, например угольная кислота. [17]
Окислительная активность элементарных веществ определяется в основном, как это видно из предыдущих рассуждений, величинами энергии сродства к электрону атома и энергии диссоциации молекулы окислителя: чем первая величина больше и чем вторая меньше, тем сильнее окислительная активность элементарного вещества. [18]
Окислительная активность хлорноватой кислоты меньше, чем хлорноватистой, так как хлорноватистая кислота легче разлагается, выделяя атомарный кислород. Окисляя вещества, хлорноватая кислота, как правило, восстанавливается до гемиоксида хлора. [19]
Окислительная активность соединений Ti ( III) выражена в меньшей степени. [20]
Окислительная активность хлорноватой кислоты меньше хлорноватистой ввиду того, что хлорноватистая кислота легче разлагается, выделяя атомарный кислород. Окисляя вещества, хлорноватая кислота, как правило, восстанавливается до хлорноватистого ангидрида. [21]
Окислительная активность элементарных веществ определяется, в основном, как это видно из предыдущих рассуждений, значениями энергии сродства к электрону атома и энергии дисео-иищни молекулы окислителя - чем первое значение больше и чем порос меньше, тем сильнее окислительная активность элсментар-пго вещества. [22]
Окислительная активность элементарных веществ определяется в основном, как это видно из предыдущих рассуждений, величинами энергии сродства к электрону атома и энергии диссоциации молекулы окислителя: чем первая величина больше и чем вторая меньше, тем сильнее окислительная активность элементарного вещества. [23]
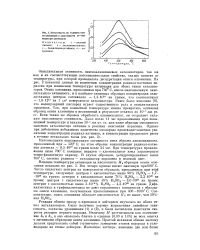 |
Кислотность по Гаммету окиси алюминия в зависимости от температуры активации. [24] |
Окислительная активность окисноалюминиевых катализаторов, так же как и их соответствующие восстановительные свойства, сильно зависят от температуры, при которой проводилась дегидратация окиси алюминия. На рис. 2 показаны данные по изменению концентрации радикал-катионов пе-рилена при изменении температуры активации для обоих типов катализаторов. Окись алюминия, прокаленная при 740е С, имела максимальную окислительную активность, и в наиболее активных образцах концентрация окислительных центров составляла - 1 4 - 1018 на грамм, что соответствует - 1 0 - 1212 на 1 см. поверхности катализатора. Ранее было показано [6], что молекулярный кислород играет существенную роль в окислительных процессах. Так, при комнатной температуре можно превратить активный образец окиси алюминия в неактивный в результате откачки до Ю-5 мм рт. ст. Если таким же образом обработать алюмосиликат, он сохраняет сильную окисляющую активность. Даже после 11 час прокаливания при повышенной температуре и вакууме 10 5 мм рт. ст. или ниже образцы смешанного окисного катализатора активны в реакции окисления перилена. [25]
Окислительная активность микробных ценозов в иле достигает максимальных значение во П ступени. [26]
Окислительная активность водородных соединений неметаллов в группах сверху вниз сильно увеличивается. [27]
Постоянная окислительная активность иона металла переменной валентности в системе позволяет изучать кинетику реакций в стационарных условиях. [28]
Окислительную активность брома и иода широко используют в различных синтезах и для анализа веществ. Иод применяют как антисептическое и кровоостанавливающее средство. [29]
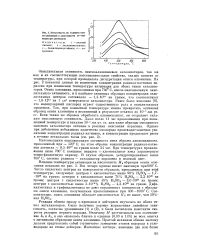 |
Кислотность по Гаммету окиси алюминия в зависимости от температуры активации. [30] |
Страницы: 1 2 3 4